题目内容
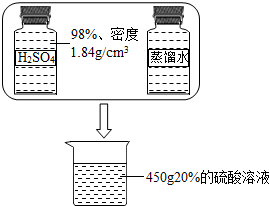
 如图为某盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
如图为某盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:(1)欲配制14.6%的稀盐酸100g,需要这种盐酸
(2)用上述配得的稀盐酸与足量的锌充分反应,可制得氢气
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据加水稀释前后溶液中溶质质量相等,由标签查得盐酸的溶质质量分数为20%,然后由稀释前后溶质质量相等的关系,计算需要这种盐酸的质量;
(2)锌与盐酸反应生成氯化锌和氢气,根据反应的化学方程式,由消耗HCl的质量计算制得氢气的质量.
(2)锌与盐酸反应生成氯化锌和氢气,根据反应的化学方程式,由消耗HCl的质量计算制得氢气的质量.
解答:解:(1)需要标签注明质量分数为20%的盐酸的质量=
=73g;
(2)设可制得氢气质量为x
Zn+2HCl═ZnCl2+H2↑
73 2
100g×14.6% x
=
x=0.4g
故答案为:(1)73g;(2)0.4g.
| 100g×14.6% |
| 20% |
(2)设可制得氢气质量为x
Zn+2HCl═ZnCl2+H2↑
73 2
100g×14.6% x
| 73 |
| 100g×14.6% |
| 2 |
| x |
x=0.4g
故答案为:(1)73g;(2)0.4g.
点评:加水稀释时,稀释前溶液的质量×溶液的溶质质量分数=稀释后溶液质量×溶液的溶质质量分数.

练习册系列答案
相关题目
化学与生产、生活、社会发展密切相关.下列说法中,不正确的是( )
| A、使用可降解塑料代替普通塑料,可以减轻“白色污染” |
| B、健身器材表面涂刷油漆,可以防止生锈 |
| C、在农业生产中将铵态氮肥与熟石灰混合使用 |
| D、在室内点煤炉时,要注意通风防止煤气中毒 |
1875年法国化学家布瓦博德朗发现了元素镓(Ga),它的原子核内质子数是31,相对原子质量是70,则它的原子核内中子数为( )
| A、31 | B、39 | C、70 | D、101 |
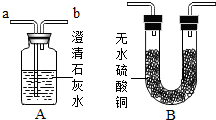 某学校化学课外活动小组,对铜制品生锈很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为Cu2(OH)2CO3,他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体,为了更清楚地了解这种黑色粉末,同学们准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体:
某学校化学课外活动小组,对铜制品生锈很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为Cu2(OH)2CO3,他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体,为了更清楚地了解这种黑色粉末,同学们准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体: