题目内容
【题目】请结合图示实验装置,回答下列问题。
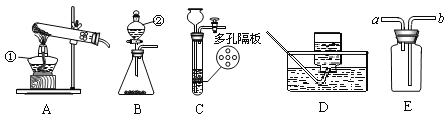
(1)写出有标号的仪器名称:①____________,②___________。
(2)用高锰酸钾制氧气选用的发生装置是___________(选填序号),反应的文字表达式为_______________________。
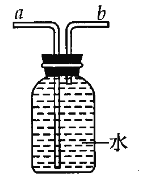
(3)若B装置中固体为二氧化锰,②加入__________可制氧气。使用仪器②的优点是____________________________。若用E装置收集氧气,气体应从___________端通入(选填“a”或“b”)。
(4)实验室可用B或C装置制二氧化碳,反应的文字表达式为___________________,C相对于B装置的优点有__________________,选用的收集装置是___________(选填序号)。
【答案】(1)①酒精灯 ②分液漏斗
(2)A 高锰酸钾![]() 锰酸钾+二氧化锰+氧气
锰酸钾+二氧化锰+氧气
(3)双氧水(或过氧化氢溶液) 控制滴加液体的量来控制反应速率(或控制反应速率) b
(4)碳酸钙+盐酸![]() 氯化钙+水+二氧化碳 控制反应的发生和停止 E
氯化钙+水+二氧化碳 控制反应的发生和停止 E
【解析】
试题分析:(2)根据反应物的状态和反应条件选择发生装置,用高锰酸钾制取氧气属固固加热型,故发生装置选A;加热高锰酸钾分解制取氧气的同时,还生成了锰酸钾和二氧化锰,故反应的表达式为:
高锰酸钾![]() 锰酸钾+二氧化锰+氧气;
锰酸钾+二氧化锰+氧气;
(3)实验室可用过氧化氢和二氧化锰制取氧气,根据题意,过氧化氢接触到二氧化锰后,反应便立即开始,不能人为控制其速率和生成氧气的量,故要控制其反应速率,可通过控制过氧化氢的加入量来实现;分液漏斗就可以控制加入液体药品的量和速率;氧气的密度比空气大,会先聚集在集气瓶的底部,故氧气从b端通入;
(4)实验室用石灰石和稀盐酸反应制取二氧化碳:碳酸钙+盐酸![]() 氯化钙+水+二氧化碳;C装置中可将石灰石放在隔板上,从长颈漏斗条件稀盐酸,当不需要反应时,可用止水夹夹住橡皮管,那么稀盐酸会进入长颈漏斗中,固体和液体分离,反应停止,故C装置可控制反应的发生和停止;二氧化碳的密度比空气大,易溶于水,故用E装置收集。
氯化钙+水+二氧化碳;C装置中可将石灰石放在隔板上,从长颈漏斗条件稀盐酸,当不需要反应时,可用止水夹夹住橡皮管,那么稀盐酸会进入长颈漏斗中,固体和液体分离,反应停止,故C装置可控制反应的发生和停止;二氧化碳的密度比空气大,易溶于水,故用E装置收集。

 快捷英语周周练系列答案
快捷英语周周练系列答案