题目内容
【题目】一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案:下列判断正确的是( ) 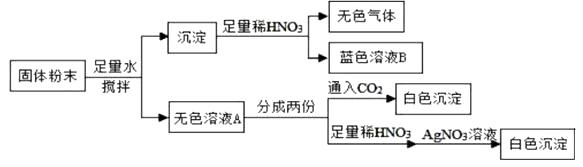
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2
【答案】B
【解析】铜离子在溶液中显蓝色,NaOH和CuCl2会生成蓝色的氢氧化铜沉淀,而氢氧化铜会与稀硝酸反应生成硝酸铜溶液;CaCO3会与稀硝酸反应生成气体,则蓝色溶液B中有硝酸铜、硝酸钙,则原固体粉末一定有CaCO3、NaOH、CuCl2和Ca(NO3)2无法确定NaNO3 和NaCl。通入CO2产生白色沉淀,说明溶液中只能够一定有硝酸钙,则溶液中必有OH-。由于有NaOH和CuCl2 , 所以无色溶液A中一定含有Na+和Cl-,之后的步骤无法确定氯化钠。 根据铜离子在溶液中显蓝色,NaOH和CuCl2会生成蓝色的氢氧化铜沉淀,而氢氧化铜会与稀硝酸反应生成硝酸铜溶液;CaCO3会与稀硝酸反应等进行分析。

练习册系列答案
相关题目