题目内容
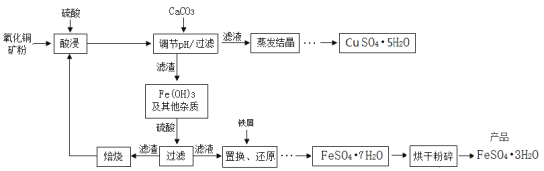
【题目】氧化铜矿石含有CuO、Cu2(OH)2CO3和Fe2O3,还含有一些不溶于水、不溶于酸的其他杂质。铜、铁是畜禽所必需的微量元素,某饲料厂联合生产硫酸铜晶体和硫酸亚铁晶体的主要工艺流程如下。
【资料】Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 |
开始沉淀的pH | 1.5 | 4.2 |
沉淀完全的pH | 3.7 | 6.7 |
请回答问题:
(1)氧化铜矿石粉碎的目的是 。
(2)写出“酸浸”中发生反应的化学方程式 (任写一个)。
(3)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒和 。
(4)右图为“硫酸亚铁干燥曲线图”,据此可确定由FeSO4·7H2O脱水得到流程中所示产品的适宜工艺条件为 、 (分别指出温度和时间)。

(5)在“调节pH/过滤”中,加入CaCO3调节溶液的pH,请说出溶液适宜的pH范围是多少并说明理由 。
【答案】⑴ 增大接触面积,加快反应的速率 ⑵ CuO+H2SO4=CuSO4+H2O⑶ 漏斗 ⑷125℃(±5)4.0h ⑸〔3.7~4.2),使Fe(OH)3 形成沉淀,而硫酸铜不形成沉淀而分离。
【解析】
试题分析:(1)反应物的接触面积与反应速率成正比,将氧化铜矿石粉碎,增大了反应物的接触面积,加快了反应速率(2)氧化铜和稀硫酸反应生成硫酸铜、水,化学方程式为CuO+H2SO4=CuSO4+H2O
(3)实验室中过滤操作需要使用的玻璃仪器有盛放溶液的烧杯,起引流作用的玻璃棒,过滤作用的漏斗,所以实验室中过滤操作需要使用的玻璃仪器有:烧杯、玻璃棒、漏斗;(4)由FeSO4·7H2O脱水制取FeSO4·3H2O,根据图硫酸亚铁干燥曲线图可知反应条件为125(±5)℃、4.0h。(5),使Fe(OH)3 形成沉淀,而硫酸铜不形成沉淀而分离,结合PH表,PH的范围为〔3.7~4.2)。