题目内容
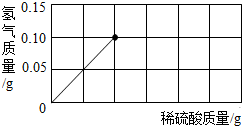 我国约在南北朝时期就开始冶炼黄铜,黄铜是铜、锌的合金,它可用来制造机器、电器零件及日用品,为了测定某黄铜样品中铜的质量分数,取10g黄铜加入到50g稀硫酸中,恰好完全反应.反应过程中生成的气体与所用稀硫酸溶液的质量关系如图所示.试计算:
我国约在南北朝时期就开始冶炼黄铜,黄铜是铜、锌的合金,它可用来制造机器、电器零件及日用品,为了测定某黄铜样品中铜的质量分数,取10g黄铜加入到50g稀硫酸中,恰好完全反应.反应过程中生成的气体与所用稀硫酸溶液的质量关系如图所示.试计算:(1)该黄铜样品中铜的质量分数;
(2)原硫酸溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:由于铜与稀硫酸不反应,故铜锌合金与稀硫酸的反应,为锌与稀硫酸的反应;
(1)利用锌与稀硫酸反应的化学方程式,计算出样品中锌的质量,进而求出样品中铜的质量,然后根据质量分数公式计算即可;
(2)利用锌与稀硫酸反应的化学方程式,计算出参与反应的H2SO4的质量,然后根据溶质质量分数公式计算即可.
(1)利用锌与稀硫酸反应的化学方程式,计算出样品中锌的质量,进而求出样品中铜的质量,然后根据质量分数公式计算即可;
(2)利用锌与稀硫酸反应的化学方程式,计算出参与反应的H2SO4的质量,然后根据溶质质量分数公式计算即可.
解答:解:设样品中锌的质量为x,参与反应的H2SO4的质量为y,
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.1g
=
,
=
,
解之得:x=3.25g,y=4.9g;
(1)样品中铜的质量分数为:
×100%=67.5%;
(2)原稀硫酸溶液中硫酸的质量分数为:
×100%=9.8%.
答:(1)样品中铜的质量分数为67.5%;(2)原稀硫酸溶液中硫酸的质量分数为9.8%.
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.1g
| 65 |
| x |
| 2 |
| 0.1g |
| 98 |
| y |
| 2 |
| 0.1g |
解之得:x=3.25g,y=4.9g;
(1)样品中铜的质量分数为:
| 10g-3.25g |
| 10g |
(2)原稀硫酸溶液中硫酸的质量分数为:
| 4.9g |
| 50g |
答:(1)样品中铜的质量分数为67.5%;(2)原稀硫酸溶液中硫酸的质量分数为9.8%.
点评:本题主要考查学生利用化学方程式和溶质质量分数公式进行计算的能力.解题时要知道铜与稀硫酸不反应,铜锌合金与稀硫酸的反应,为锌与稀硫酸的反应.然后根据化学方程式进行计算,问题即可迎刃而解.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
分类学习是化学学习的重要思想方法,下列物质分类错误的一组是( )
| A、S P C |
| B、CH4 C2H5OH C6H12O6 |
| C、NaCl CaCO3 Na2CO3 |
| D、空气 H2SO4 HCl |
科学家设想利用道路来收集太阳能进行发电,供电动汽车和路灯使用.方法是在路基上铺设覆盖有太阳能电池的水泥板,再在太阳能电池上覆盖透明的玻璃作为路面,这个设想要能实际使用,对玻璃的选择,下列( )不是主要需考虑的因素.
| A、玻璃表面粗糙程度 |
| B、玻璃强度 |
| C、玻璃颜色 |
| D、玻璃的隔音效果 |
铁是一种应用广泛的金属,下列有关铁的说法中,正确的是( )
| A、铁丝在氧气中燃烧生成氧化铁 |
| B、铁不能与稀硫酸反应生成氢气 |
| C、铁是地壳里含量最多的金属元素 |
| D、用铁锅炒菜可使食物中增加微量元素 |
 甲、乙、丙三种物质的溶解度曲线如图所示.根据溶解度曲线回答有关问题:
甲、乙、丙三种物质的溶解度曲线如图所示.根据溶解度曲线回答有关问题: