题目内容
某学习小组测定黄铜屑(锌铜合金)的组成,取一定量黄铜屑放入锥形瓶中,并加入足量稀硫酸,并迅速放在电子天平上进行称量。不同时间电子天平的读数如下表所示(不考虑H2O逸出及溶液温度变化):
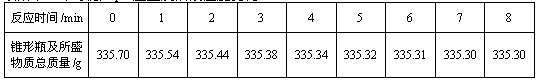
(1)反应生成H2的总质量为_______g。
(2)若要计算黄铜屑中锌的质量分数,还缺少的数据是_____________。若该数据用a表示,求黄铜屑中锌的质量分数(写出计算过程)。
解:(1)反应生成H2的总质量:335.70g-35.30g=0.4g
(2)黄铜屑的总质量 设Zn的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.4g
![]() x=13g
x=13g
黄铜屑中锌的质量分数:![]()

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
某学习小组的同学们用下图所示装置测定黄铜屑(锌铜合金)的组成,他们首先取一定量的黄铜屑放入锥形瓶中,并加入足量的稀硫酸.然后观察到不同时间电子天平的读数如下表所示(不考虑水逸出):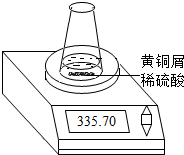
(1)反应生成氢气的总质量为 g.
(2)若要计算黄铜屑中锌的质量分数,还缺少的数据是 .
(3)若该数据用a表示,求出黄铜屑中锌的质量分数(写出计算过程).

| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 烧杯及所盛 物质总质量/g |
335.70 | 335.54 | 335.44 | 335.38 | 335.34 | 335.32 | 335.31 | 335.30 | 335.30 |
(2)若要计算黄铜屑中锌的质量分数,还缺少的数据是
(3)若该数据用a表示,求出黄铜屑中锌的质量分数(写出计算过程).
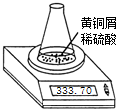 测定黄铜屑(锌铜合金)的组成有多种方案.某学习小组用图示装置测定黄铜屑中锌的质量分数,取一定量黄铜屑放入锥形瓶中,并加入足量稀硫酸.不同时间电子天平的读数如下表所示(不考虑H2O逸出及溶液温度变化):
测定黄铜屑(锌铜合金)的组成有多种方案.某学习小组用图示装置测定黄铜屑中锌的质量分数,取一定量黄铜屑放入锥形瓶中,并加入足量稀硫酸.不同时间电子天平的读数如下表所示(不考虑H2O逸出及溶液温度变化):| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 锥形瓶及所盛物质总质量/g | 335.70 | 335.54 | 335.44 | 335.38 | 335.34 | 335.32 | 335.31 | 335.30 | 335.30 |
(2)若要计算黄铜屑中锌的质量分数,还缺少的数据是
(3)请你再设计一个测定黄铜屑中锌的质量分数的方案.
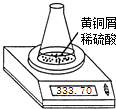 测定黄铜屑(锌铜合金)的组成有多种方案.某学习小组用图示装置测定黄铜屑中锌的质量分数,取一定量黄铜屑放入锥形瓶中,并加入足量稀硫酸.不同时间电子天平的读数如下表所示(不考虑H2O逸出及溶液温度变化):
测定黄铜屑(锌铜合金)的组成有多种方案.某学习小组用图示装置测定黄铜屑中锌的质量分数,取一定量黄铜屑放入锥形瓶中,并加入足量稀硫酸.不同时间电子天平的读数如下表所示(不考虑H2O逸出及溶液温度变化):
| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 锥形瓶及所盛物质总质量/g | 335.70 | 335.54 | 335.44 | 335.38 | 335.34 | 335.32 | 335.31 | 335.30 | 335.30 |
(2)若要计算黄铜屑中锌的质量分数,还缺少的数据是________.若该数据用a表示,求黄铜屑中锌的质量分数(写出计算过程).
(3)请你再设计一个测定黄铜屑中锌的质量分数的方案.