��Ŀ����
ijѧϰС�����ʵ�������չ�������̼����ļ�ʯ�ҳɷֽ������о���
���������ϡ�
�ټ�ʯ����CaO��NaOH �Ĺ������ͨ���������ն�����̼���������壮
�ڼ��Ե�Na2CO3��Һ���������Ե�CaCl2��Һ�������ֽⷴӦ��
��������롿
�ü�ʯ�ҵ���Ҫ�ɷֿ��ܺ����� ����Ca��OH��2��CaCO3��NaOH���� ����
����Ʒ������ռ�֤�ݡ�
��1����ͬѧ���ձ��з��������ļ�ʯ����Ʒ��������������ˮ��ֽ��裬�����а�ɫ��������ͬѧ��Ϊ��Ʒ��һ������CaCO3����ͬѧ��Ϊ���Ľ��۲�ȷ��ԭ���ǣ��� �����ѧ����ʽ����
��2����ͬѧ��һ�����ʵ�鲢������֤���������£�
| ʵ����� | ʵ������ | ʵ����� |
| �ٴӼ�ͬѧ���ձ���ȡ�����ϲ���Һ���Թ��У������еμ������� ����Һ�� | �а�ɫ�������� | ���ɰ�ɫ�����Ļ�ѧ����ʽΪ�� �� ���� |
| �ڹ��ˣ�����Һ�еμ���ɫ��̪��Һ�� | ���������� | ͨ��ʵ�鼰��������Ʒ�в����У� �� ���� |
��1����ͬѧ��һ�����������ʵ��װ�ã�ͨ������Bװ�õ������仯��ȷ����Ʒ�ijɷּ����������������ã�ÿ������ȫ��Ӧ����������

���ʵ�鷢�ֲⶨ�����ʱƫ����ʱƫСƫ��Է�������Ҫԭ���� ��
��2������ʦ��ָ������ͬѧ������ʵ��װ�ã������½�����ʵ�飬�������£�

�ټ��װ�������ԣ���5.06g�������Ʒ������ƿ�У�
�ڴ���b���ӵ���a����������һ�����Ŀ������رջ���b��
�۳���ʢ����������Ũ��Һ��Dƿ������
������ƿ����μ���ϡ���������ٲ������ݣ�
�ݴ���b���ӵ���a����������һ�����Ŀ�����
����Dƿ����������2.2g��
ͨ�������������֪��5.06g��Ʒ�и��ɷּ������� ������
��������롿CaO Na2CO3����Ʒ������ռ�֤�ݡ���1��Na2CO3+Ca��OH��2=CaCO3��+2NaOH
��2��CaCl2��Na2CO3+CaCl2=CaCO3��+2NaCl��Ca��OH��2��NaOH�� CaO��
�����������ۡ���1����ƿ�в�����CO2δ�����ջᵼ�½��ƫС�����ӷ����������ἰ�����ж�����̼��ˮ������������ᵼ�½��ƫ��ÿ��ʵ�����������ۺ����ã�������CO2�������ڻӷ����������ἰ�����ж�����̼ˮ�����������½��ƫС����֮����ƫ��2��CaCO3��4�� Na2CO3��1.06g��
���������������������롿�ü�ʯ��������������ˮ��Ӧ�����������ƣ����������������̼��Ӧ����̼��ƺ�ˮ�������������������̼��Ӧ����̼���ƺ�ˮ�����ն�����̼�����Ҫ�ɷֿ��ܺ��к��� CaO��Ca��OH��2��CaCO3��NaOH�� Na2CO3����Ʒ������ռ�֤�ݡ���1����ͬѧ���ձ��з��������ļ�ʯ����Ʒ��������������ˮ��ֽ��裬�����а�ɫ��������ͬѧ��Ϊ��Ʒ��һ������CaCO3����˵����ȷ����Ϊ��ʯ����Ʒ�п��ܺ���̼���ƺ��������ƣ�̼�������������Ʒ�Ӧ������̼��Ƴ�������ѧ����ʽΪ Na2CO3+Ca��OH��2=CaCO3��+2NaOH����2����ͬѧҪ��֤���Ƿ���̼���ƣ���̼�������Ȼ��Ʒ�Ӧ������̼��ư�ɫ��������˿ɴӼ�ͬѧ���ձ���ȡ�����ϲ���Һ���Թ��У������еμ����� CaCl2��Һ���а�ɫ�������ɣ�˵������̼���ƣ���ѧ����ʽΪNa2CO3+CaCl2=CaCO3��+2NaCl��Ȼ����ˣ�����Һ�еμ���ɫ��̪��Һ������������˵����Ʒ��һ�������м������ʣ����һ������Ca��OH��2��NaOH�� CaO�������������ۡ���1����ͬѧ���ʵ��װ�ã���Ʒ�м������ᣬͨ������Bװ������������Һ�������仯��ȷ�����ɵĶ�����̼���������Ӷ�ȷ����Ʒ�ijɷּ�����������ƿ�в�����CO2δ�����ջᵼ�½��ƫС�����ӷ��������Ȼ��⼰�����ж�����̼��ˮ������������ᵼ�½��ƫ��ÿ��ʵ�����������ۺ����ã�������CO2�������ڻӷ��������Ȼ��⼰�����ж�����̼ˮ�����������½��ƫС����֮����ƫ��
��2������Ʒ��̼��������Ϊx��̼�������Ϊ5.06g��x
Na2CO3+H2SO4�TNa2SO4+H2O+CO2��
106 44
x 
CaCO3+H2SO4�TCaSO4+H2O+CO2��
100 44
5.06g��x 
 +
+ =2.2g
=2.2g
x=1.06g
̼�������Ϊ5.06g��1.06g=4g
���㣺ʵ��̽�����ʵ���ɳɷ��Լ�������

ij��ѧ��ȤС���ڻ�ѧʵ���ҷ���һƿû�б�ǩ�ĵ���ɫ��ĩ��ͬѧ�Ƕ�̽���÷�ĩ����Ũ����Ȥ��������ʦ��ָ���½���̽�����
��������⡿���ֵ���ɫ��ĩ��ʲô����ʲô���ʺ���;��
���������ϡ������ǵ���ɫ��ĩ��������ˮ��
�ڹ������ƣ�Na2O2���ǵ���ɫ��ĩ������ˮ������ˮ��Ӧ������������ɴ���DZˮͧ��һ�㶼Ҫ��װʢ�Ź������ƣ�Na2O2��������װ�á�
��������̽����
���룺����ɫ��ĩ�����ǣ�a����b���������ƣ�c����������ƵĻ����
��ʵ������ۡ�
| | ʵ����� | ʵ������ | ʵ����� |
| ���� | ��һ֧�ྻ���Թ��м�����������������ɫ��ĩ���ټ�������������ˮ������� | | ����a��c������������b������ |
��������⡿���������Ƿ�Ϊһ�������������˺������������巢����Ӧ��
��������롿�����������˺�����N2��CO2��ˮ������Ӧ������������
������ʵ�顿
ʵ�����֤���������뵪����Ӧ������������

����ͬѧ�������ͼ��ʾװ�ã�
��1��ʵ�������ۣ��۲쵽____________�����жϹ��������뵪��û�з�����Ӧ��
ʵ�����֤����������ˮ������Ӧ������������
����ͬѧ���������ͼ��ʾװ��
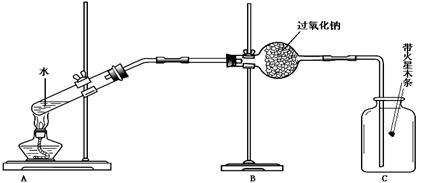
��2������Aװ�õ�������____________��
��3��ʵ�������ۣ������ǵ�ľ����ȼ��
ʵ�����֤���������������̼��Ӧ�������������������ʦ��ָ����Ҳ���������ͼ��ʾװ�á���������ϡ����Ļӷ���
| ʵ����� | ��Ҫʵ������ | ʵ����ۼ����� | |
| �� | ���װ�õ������ԡ� ��װ���м���ҩƷ�� | | װ�õ����������á� |
| �� | ��Һ©����������Aװ���л�������ϡ���ᡣ | Aװ���й۲쵽��������__________�� Cװ���������ݳ��֡� | Aװ���з�����Ӧ�Ļ�ѧ����ʽΪ________�� ��2�֣� |
| �� | һ��ʱ����ô����ǵ�ľ����D�ڽ��м��顣 | �����ǵ�ľ����ȼ�� | ���������������̼��Ӧ������������ |

��4��ʵ���¼
��ʵ�鷴˼��
�ź�ͬѧ��ʵ�������������ʣ���ʵ�鲻��֤��������̼���������ȷʵ�����˷�Ӧ������Ϊ����������_____ ___������ش���θĽ���ʵ�� ��
ij�ѧʵ��ν�������ε�����ʵ�顣
���������ָʾ����
��1��ȡ�����ϰ��˺Ͱײ�Ҷ�����ֱ�����в��е��ã�����ƾ����ݣ���ɴ�������ݳ���֭Һ�������ֱ�װ�ô��á�
��2��ȡ��֧�Թֱܷ���NaOH��Һ��ϡ�������ʵ�飬�۲쵽������ͼ����¼���£�
| | NaOH��Һ | ϡ���� | ƻ��֭ |
| �ϰ���֭Һ | ����ɫ | �ں�ɫ | ��ɫ |
| �ײ�֭Һ | ����ɫ | �ܵ���ɫ | ����ɫ |
����Ϊ����֭Һ�У����ʺ������ָʾ�������� ����
��3������ƻ��֭������ͬʵ�飬�����¼���ϱ�����ƻ��֭��Һ���� ���ԡ�
������ε����ʡ�
��һ��ѧ������CuSO4��NaOH��Һ�ķ�Ӧ���۲쵽���������� ����
�ڶ���ѧ������BaCl2��Na2CO3��Һ�ķ�Ӧ����Ӧ�ķ���ʽΪ�� ����
�Ӹ��ֽⷴӦ�������۱����Ͽ����кͷ�Ӧ��ʵ�ʿ�������ͼ1��ʾ����ô����ͼ2����н�CuSO4��NaOH��Һ�ķ�Ӧ����ʾ��ͼ����������
����Һ��̽����
ʵ�����������ͬѧ��ȫ������Һ���е���һ����Һ���У���ѧ��ȤС�����Һ���й��ˣ��õ���ɫ��Һ����һ��̽����ɫ��Һ�ijɷ֡�
��������⡿��Һ�����ʳ���NaCl�⣬����ʲô���ʣ�
��������롿����٣�BaCl2������ڣ�Na2SO4������ۣ�NaOH������ܣ�BaCl2��NaOH�����룺��Na2CO3��Na2SO4�����룺��Na2SO4��NaOH�����룺��Na2CO3��Na2SO4���� ����
��ʵ��̽����
��1��ȡ�����μ��ϰ���Ҷ֭������ɫ��С���ж�һ����NaOH��С����ͬ�⣬�������� ������2��ȡ��������������ϡ���ᣬ����������������� ��һ����������
��3��Ϊȷ������Һ����ɣ����貹���ʵ���ǣ��� �������۲쵽��ɫ�����������ɫ��Һ��������� ����
��������ṩ��ʵ��װ�ú�ҩƷ������ʵ���������Ʊ���̽����
A B C D E F
���ṩҩƷ��������ء�ϡ���ᡢ����ʯ
����Ϥ����������д������������ƣ���_________����________��
���Ƚ��о����������ṩ��ҩƷ����д�±���
| ���� | ��Ӧ��״̬ | ��Ӧ���� | �ռ����������� | |
| ������̼ | �����Һ�� | ���� | �����ſ����� | CO2�ܶȱȿ����� |
| ���� | ���� | ���� | ��ˮ�� | ��______________ |
| ��_____________ | O2�ܶȱȿ����Դ� | |||
��ʵ���о�����1���ü��ȸ�����صķ�����ȡ������Ӧѡ�÷���װ��A��д���÷�Ӧ�����ֱ���ʽ__________________________��
��2��������ijͬѧ�ü��ȸ��������ȡ������������ˮ���ռ��IJ���ʵ����������в���������___��
A���ȼ��װ�õ������ԣ����ҩƷ
B���Ƚ��������뼯��ƿ��������Թ�
C��ʵ������Ƚ������Ƴ�ˮ�棬��Ϩ��ƾ���
��3��ʵ������ȡ����___װ����ϣ�����ĸ��ţ�����ȡ������̼��д��ʵ������ȡ������̼�����ֱ���ʽ____________________________________��
����˼С�ʵ������ȡ����ķ���װ�ú��ռ�װ�õ�ѡ�����ݣ�
����װ�õ�ѡ�����ݡ���_________��_________��
�ռ�װ�õ�ѡ�����ݡ��������______��������ˮ�е�______���������ܷ��������ˮ��Ӧ������չӦ�á�ʵ������п����ϡ���ᷴӦ��ȡ������Ӧѡ�õķ���װ����B��C�� C��B��Ƚϣ����ŵ���_______________________���������ܶ���С�����壬������ˮ����ѡ�õ��ռ�װ��Ϊ___������ĸ��ţ���




