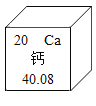
题目内容
【题目】某研究性学习小组利用下列装置进行气体的制取,请回答:
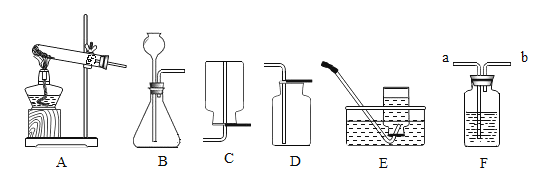
(1)选用A装置制取氧气的化学方程式是____________。
(2)A、E连接制取氧气,收集的氧气不纯的原因是____________(写一点即可)。
(3)若用过氧化氢溶液制取一瓶干燥的氧气,需要用到装置F,则装置F中应加入的物质是_______,气体应从________端通入(填“a”或"b”)。
(4)实验室制取二氧化碳选择的发生装置和收集装置是________(填序号),选择该发生装置的依据是____________________。
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ 导管口刚有气泡冒出就开始收集(或集气瓶没有装满水) 浓硫酸 a BD 固体与液体在常温下反应
K2MnO4+MnO2+O2↑ 导管口刚有气泡冒出就开始收集(或集气瓶没有装满水) 浓硫酸 a BD 固体与液体在常温下反应
【解析】
(1)实验室用A装置制取氧气,属于固体加热型,试管口放有一团棉花,采用加热高锰酸钾的方法,高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4![]() K2MnO4+MnO2+O2↑,故填:2KMnO4
K2MnO4+MnO2+O2↑,故填:2KMnO4![]() K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
(2)用排水法收集氧气的合适时机是:气泡连续均匀冒出时收集,以防收集的氧气不纯,因此A、E连接,制取的氧气不纯的可能原因是:导管口刚有气泡冒出就开始收集;另外集气瓶内若没装满水,留有气泡,也会使收集的气体不纯,故填:导管口刚有气泡冒出就开始收集(或集气瓶没有装满水)。
(3)用过氧化氢溶液制取一瓶干燥的氧气,则F装置是干燥装置,则装置F中应放入的物质是浓硫酸,氧气从长管进入,可以得到充分的干燥,故填:浓硫酸;a。
(4)碳酸钙和稀盐酸反应不需要加热,应该用B装置作为发生装置;二氧化碳能够溶于水,密度比空气大,可以用向上排空气法收集,即用D装置收集,故填:BD;固体与液体在常温下反应。
。

 能考试期末冲刺卷系列答案
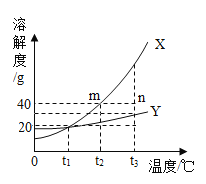
能考试期末冲刺卷系列答案【题目】下列图像不能正确反映对应变化关系的是
|
|
|
|
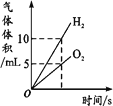
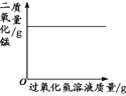
A.将水通电电解一 段时间 | B.加热一定量的高 锰酸钾固体 | C.向两份相等质量的块状大理石和粉末状大理石中分别加入过量的等浓度的稀盐酸 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D
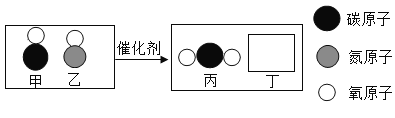
【题目】学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:Fe2O3能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
(猜想)I.Fe2O3是反应的催化剂,反应前后__;
II.Fe2O3参与反应产生O2,反应前后质量和化学性质发生了改变;
III.Fe2O3不是催化剂、也不参与反应,反应前后质量和化学性质不变.
(查阅资料)Fe2O3属于碱性氧化物,能够与稀盐酸反应生成氯化铁;氯化铁溶液显棕黄色.
(实验)用天平称量 0.3gFe2O3,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
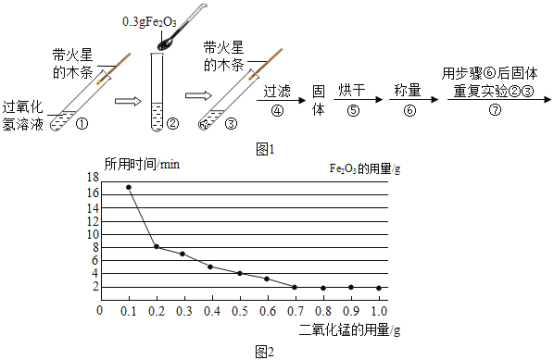
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
__,带火星的木条复燃. | __ | 溶液中有气泡放出, __ | 猜想I成立; 猜想II、III不成立. |
(2)步骤①的目的是__.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、__.
(4)过氧化氢能被Fe2O3催化分解放出O2的化学方程式为__.
(拓展)
(1)要探究步骤⑤做过催化剂的Fe2O3其它化学性质,还应补做的实验是__(写一种).
(2)该同学为了探究Fe2O3的用量对H2O2分解速率的影响.每次均用30mL 10%的H2O2溶液,使用不同质量的Fe2O3作催化剂,测定每次收集到500mL O2所用的时间.结果如图(其他实验条件相同),由图可知,Fe2O3的用量对H2O2分解速率影响的规律是:
①__;
②Fe2O3的用量超出一定范围后,其用量再增大,反应速率不再继续加快.