题目内容
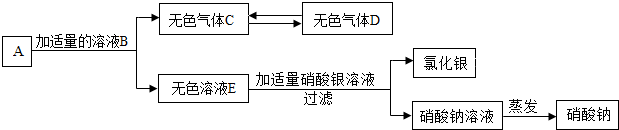
白色粉末A,由Na2SO4、Na2CO3、BaCl2、NaCl中的三种物质混合而成.把A加入到适量水中后,可得到白色沉淀B和溶液C,则:(1)若B能全部溶于稀硝酸时,A的成分为 ;
(2)若B只能部分溶于稀硝酸时,A的成分为 ;
(3)若B不能溶于稀硝酸时,A的成分为 ;
(4)溶液C中一定存在的溶质是 .
【答案】分析:本题中所给的四种物质都是盐类,并且溶于水后能够产生白色沉淀,而能够产生白色沉淀的反应为:碳酸钠和氯化钡反应生成碳酸钡、硫酸钠和氯化钡生成硫酸钡,其中硫酸钡不溶于稀硝酸,而碳酸钡可以溶于稀硝酸,所以可以得出在四种物质中至少含有碳酸钠、和硫酸钠中的一种物质,而氯化钡是一定含有的,可以据此作出解答.
解答:解:(1)若白色沉淀完全溶解,以为硫酸钡不溶于稀硝酸,所以可以知道该白色沉淀为碳酸钠和氯化钡反应生成的碳酸钡,所以没有硫酸钠,即该白色粉末为:碳酸钠、氯化钡和氯化钠;
(2)若B只能部分溶于稀硝酸,则该白色沉淀为碳酸钡和硫酸钡的混合物,所以A的成分为硫酸钠、碳酸钠和氯化钡;
(3)若B不能溶于稀硝酸,则该白色沉淀为硫酸钡,所以可以知道一定没有碳酸钠,即该白色粉末为:硫酸钠、氯化钡和氯化钠的混合物;
(4)由于氯化钡是一定存在的,所以当氯化钡和硫酸钠或是碳酸钠反应时必然要生成氯化钠,所以在溶液C中一定含有氯化钠.
故答案为:(1)Na2CO3、BaCl2、NaCl;
(2)Na2SO4、Na2CO3、BaCl2;
(3)Na2SO4、BaCl2、NaCl;
(4)NaCl.
点评:熟练掌握常见的盐之间及盐与盐之间发生的化学反应,知道碳酸钡和硫酸钡都是白色沉淀,其中硫酸钡是既不溶于水也不溶于稀硝酸的白色沉淀.
解答:解:(1)若白色沉淀完全溶解,以为硫酸钡不溶于稀硝酸,所以可以知道该白色沉淀为碳酸钠和氯化钡反应生成的碳酸钡,所以没有硫酸钠,即该白色粉末为:碳酸钠、氯化钡和氯化钠;
(2)若B只能部分溶于稀硝酸,则该白色沉淀为碳酸钡和硫酸钡的混合物,所以A的成分为硫酸钠、碳酸钠和氯化钡;
(3)若B不能溶于稀硝酸,则该白色沉淀为硫酸钡,所以可以知道一定没有碳酸钠,即该白色粉末为:硫酸钠、氯化钡和氯化钠的混合物;
(4)由于氯化钡是一定存在的,所以当氯化钡和硫酸钠或是碳酸钠反应时必然要生成氯化钠,所以在溶液C中一定含有氯化钠.
故答案为:(1)Na2CO3、BaCl2、NaCl;
(2)Na2SO4、Na2CO3、BaCl2;
(3)Na2SO4、BaCl2、NaCl;
(4)NaCl.
点评:熟练掌握常见的盐之间及盐与盐之间发生的化学反应,知道碳酸钡和硫酸钡都是白色沉淀,其中硫酸钡是既不溶于水也不溶于稀硝酸的白色沉淀.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目