题目内容
【题目】我国首套面向中小学海洋教育教本将普及丰富的海洋知识,我国提出建设海洋强国的蓝色经济发展战略,丰富的海洋资源需要综合利用与科学开发。则回答:
(1)海水淡化:目前海水淡化普遍采用的方法是____,证明得到的水是淡水的物理方法是____。
(2)海水制盐:①制粗盐:从卤水中提取粗盐用的结晶方法是____。②粗盐纯化:将粗盐提纯可以得到纯净的NaCl。③配制溶液:欲用纯净的NaCl配制100g0.9%的生理盐水,需要NaCl的质量为___克。配制该溶液时需要的玻璃仪器有_____。如果配制的溶液的溶质质量分数高于0.9%,你认为可能的原因是____。
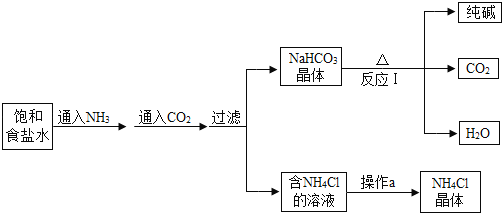
(3)海水制碱:利用氨碱法制得纯碱的工业流程图如下:
![]()
完成上图中三个步骤的内容:其中①通入气体的化学式为____;②通入物质的名称为_____;如果这两步反过来,二氧化碳的吸收率会降低。这是因为_____。③中的实验步骤为____。
(4)海水制镁:工业上一般用电解熔融状态的氯化镁制取金属镁,请写出该反应的化学方程式为______。
【答案】多级闪急蒸馏法(或蒸馏法) 加热蒸发后无残留物或液体不导电,则是淡水 蒸发结晶 0.9 烧杯、量筒、玻璃棒、胶头滴管 用量筒量取水时错误,如取水时俯视读数等 NH3 二氧化碳 氨气溶于水形成碱性溶液,更易于吸收二氧化碳 加热(或热解) MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
【解析】
(1)海水淡化:海水淡化的方法主要是将杂质除去,将水提炼出即可,可以用多级闪急蒸馏法(或蒸馏法);证明淡水的方法可用加热蒸发无晶体析出或者利用纯水不导电或利用AgNO3溶液证明无Cl-等;
(2)①因为氯化钠的溶解度随温度的变化不大,所以采用蒸发溶剂法结晶;
③根据溶质的质量=溶液×溶液质量分数,可知溶质的质量为0.9%×100=0.9g;烧杯用来溶解固体配制溶液,量筒用来量取水的体积,玻璃棒可以搅拌加速溶解,胶头滴管在量筒量取水的条件时用来校准体积;配制溶液的溶质质量分数高于0.9%可能是量取水俯视读数,即溶剂少了(答案合理即可);
(3)根据题中所给生成物进行分析,要制备饱和氨水肯定是将氨水通入食盐水中,由饱和的氨水食盐溶液制备碳酸氢钠,根据物质的性质和元素守恒知应通入二氧化碳气体;碳酸氢钠受热易分解变为碳酸钠;先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通过二氧化碳,其原因是能够更多、更快的吸收二氧化碳;
(4)电解熔融状态的氯化镁制取金属镁,该反应的化学方程式为:MgCl2![]() Mg+Cl2↑。
Mg+Cl2↑。

【题目】某白色固体可能由BaC12、NaOH、Na2CO3、Na2SO4中的一种或几种物质组成,某兴趣小组的同学为确定该白色固体的成分,进行了如下的实验探究,请你参与并回答相关问题。
I.初步探究:小金同学设计的实验过程及现象如下图所示。
(查阅资料)BaC12溶液显中性。

(初步结沦)(1)原白色固体中一定有的物质是_________,一定没有的物质是_________。
(2)M溶液中的溶质一定有__________,一定没有氯化钡。
(交流讨论)小英同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠。若要进一步确定,需对溶液M继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究:
(提出问题)无色溶液M中有氢氧化钠吗?
(猜想与假设)猜想一:有NaOH
猜想二:没有NaOH
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
A.取无色溶液M于试管中,加入过量的氯化钡溶液,振荡,静置 | _______________ | 证明溶液M中有碳酸钠并被除尽 |
B.取实验A所得上层清液于试管中,加入_______________。 | _____________ | 猜想一正确 |
在老师的指导下,同学们通过交流、讨论、实验,圆满地完成了这次探究活动。
【题目】利用如图所示装置进行实验。从A或B中任选一个作答,若均作答,按A计分。
A | B |
A处观察到的现象为________,产生该现象的原因为________。 |
A处观察到的现象为_______,产生该现象的原因为________。 |