题目内容
【题目】我国第四套人民币硬币中使用到镍(Ni)、铜、铁等金属.某兴趣小组决定探究Ni、Fe、Cu的金属活动性顺序.
(1)[查阅资料]镍能与稀硫酸反应,生成可溶于水的NiSO4,并放出氢气.
①写出镍与稀硫酸反应的化学方程式 .
②结合所学知识, (填“能”或“不能”)直接比较出Ni、Fe的金属活动性强弱.
(2)[探究实验](所用金属片均已用砂纸打磨).
实验步骤 | 实验现象 | 结论 |
相同浓度的NiSO4溶液 | 铁片表面有固体析出,铜片表面 . | 三种金属活动性由强到弱的顺序为: . |
(3)[实验反思]用镍片、硫酸亚铁溶液和 (填化学式)溶液通过实验也能判断Fe、Ni、Cu的金属活动性顺序.
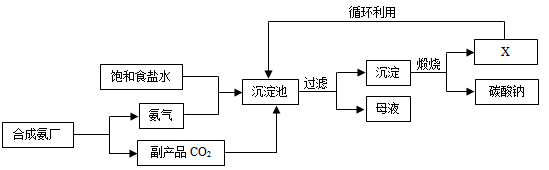
(4)[迁移应用]某化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,此外还有一些不溶性杂质.若废液直接排放到下水道不仅造成重金属污染,而且造成浪费,该校化学兴趣小组同学设计了如图废液处理方案,请回答有关问题:
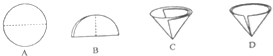
①废液在加入金属X前需进行过滤,过滤时需要将圆形滤纸折叠处理.如图不该出现的情况是 .
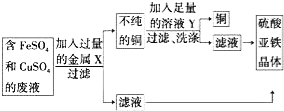
②加入过量金属X发生反应的化学方程式为 ,溶液Y是 .
【答案】(1)①Ni+2HCl=NiCl2+H2↑;②不能;
(2)没有明显现象;Fe、Ni、Cu;
(3)CuSO4;(4)①D;②Fe+CuSO4=FeSO4+Cu;稀硫酸;
【解析】(1)①根据查阅的资料,Ni显正二价,故与盐酸反应时生成二价镍盐,同时生成氢气,反应的方程式为:Ni+2HCl=NiCl2+H2↑;
②镍和铁都能与盐酸或稀硫酸反应,并放出氢气,因此根据二者产生气泡的速率快慢比较二者的活动性强弱;
(2)因为镍和铁都在氢的前面,故铜不能置换出镍,观察到的现象是:没有明显现象;铁可以置换出镍,因此三种金属活动性由强到弱的顺序为:Fe、Ni、Cu;
(3)金属和盐溶液发生置换反应的规律是排在前面的金属能把排在后面的金属从其盐溶液中置换出来,所以利用金属和盐溶液的置换反应进行验证.
故可选择中间的金属与其它两种金属的盐溶液能否发生置换反应进行验证:在两只试管中分别放入打磨光亮的镍片,再加入硫酸亚铁溶液和硫酸铜溶液中;现象为:在硫酸亚铁溶液中的镍片没有变化,在硫酸铜溶液中的镍片表面出现红色物质;
(4)①操作中需要将圆形滤纸折叠处理,D中的滤纸,接口处出现缝隙,液体会直接的进入下面的烧杯,故不该出现.
②为回收废液中的Cu2+并得到较为纯净的FeSO4溶液,需向废液中加入过量的铁粉与硫酸铜发生置换反应.发生反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;为除去混在铜粉里的铁粉并且得到FeSO4溶液,把金属混合物放入足量的稀硫酸并过滤.

 阅读快车系列答案
阅读快车系列答案