题目内容
【题目】下列四个图象的变化趋势,能正确描述对应操作的是( )
A. 往碳酸钠溶液中滴加稀盐酸
往碳酸钠溶液中滴加稀盐酸
B.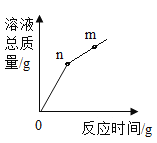 将稀盐酸滴入装有铁锈的烧杯中
将稀盐酸滴入装有铁锈的烧杯中
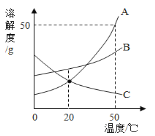
C. 向饱和的石灰水中加入足量的生石灰
向饱和的石灰水中加入足量的生石灰
D. 将锌粉加入其硫酸铜溶液中
将锌粉加入其硫酸铜溶液中
【答案】C
【解析】
A、向一定质量的碳酸钠溶液中不断滴加稀盐酸,开始为碳酸钠溶液,显碱性,pH>7,当二者恰好完全反应时,溶液的pH=7,当稀盐酸过量时,溶液的pH<7,故错误;
B、将稀盐酸滴入装有铁锈的烧杯中,氧化铁先和盐酸反应生成氯化铁和水,溶液增加的质量就是参加反应氧化铁的质量,氧化铁反应完后,铁再和盐酸反应生成氯化亚铁和氢气,溶液增加的质量就是参加反应铁的质量减去生成氢气的质量,所以开始阶段溶液质量增加的幅度大,氧化铁反应完后溶液质量增加的幅度相对小,直到反应完成溶液的质量不再增加,故错误;
C、由于氧化钙能与水发生反应生成氢氧化钙,氧化钙反应消耗了饱和溶液中的水,而使饱和溶液因减少溶剂水而析出固体,剩余固体的质量不断减少至不再变化为止,故正确;
D、将锌粉加入其硫酸铜溶液中,锌和硫酸铜反应生成铜和硫酸锌,每65份质量的锌参加反,同时生成64份质量的铜,剩余固体质量一直减少到反应停止,故错误;
故选C。

【题目】有一包白色固体,可能含有氯化钠、氢氧化钠、碳酸钠、硫酸钠和硝酸钡中的一种或几种,为探究其组成,某合作学习小组设计方案并进行了如下实验:
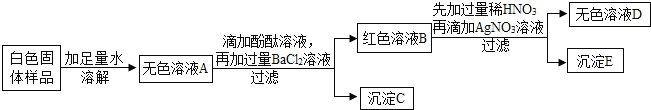
(1)小晶同学通过上述实验推知:白色固体样品中一定不含有____________(用化学式表示,下同)。
(2)为确定白色固体样品中可能存在的物质,小燕对沉淀C进行实验。
实验操作 | 现象 | 结论 |
取少量沉淀C于试管中,加入过量稀硝酸。 | ___________。 | 白色固体样品中一定含有碳酸钠和硫酸钠。 |
(3)上述实验中红色溶液B的溶质,除酚酞外,还一定含有______________________,用化学方程式表示红色溶液B变成无色溶液D的原因:_____________________________。
(4)小虎同学认为白色固体中还有物质不能确认其是否存在,经过小组讨论后得出一致意见:如要确认,只需将上述实验方案中所加的一种试剂换为另一种试剂即可,你认为修改方案为_______________。
【题目】碳和碳组成的化合物是初中化学研究的重要内容,请认真阅读题目,完成下列问题。
(1)现代生活倡导“低碳生活”,主要是为了减少_______(填化学式)的排放量。
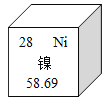
(2)组成化合物种类最多的元素是碳,如图所示,是元素周期表的一格。下列说法不正确的是__________。

A碳属于非金属元素 B碳元素的相对原子质量为12.01g
C碳原子中含有6个中子 D碳元素位于元素周期表的第ⅥA族
(3)吹不灭的蜡烛实验中,蜡烛中混有镁粉。已知镁条在二氧化碳气体中燃烧生成碳和氧化镁,请书写其化学方程式为__________;根据上述内容,你对燃烧知识有何新认识_________。
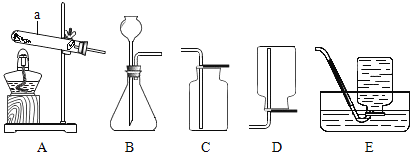
(4)如图是初中化学中常见仪器装置,回答下列问题:

①用大理石和稀盐酸制取并收集二氧化碳,可选用的装置是________,为防止气体从发生装置泄漏的必要措施是___________。
②F装置有多种用途。除去一氧化碳中的二氧化碳时,瓶中液体可以是_________。
A浓硫酸 B烧碱溶液 C浓盐酸 D饱和的碳酸氢钠溶液
(5)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用45g石灰石样品,把200g稀盐酸分四次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后过滤、干燥等操作,最后称量,得实验数据如下表:
稀盐酸的用量 | 第一次加入50g | 第二次加入50g | 第三次加入50g | 第四次加入50g |
剩余固体的质量 | 35g | 25g | 15g | 9g |
请计算该盐酸的溶质质量分数________。