题目内容
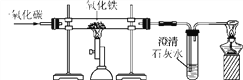
【题目】根据下列装置图回答问题:
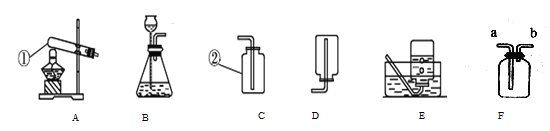
(1)写出编号仪器①和②的名称:① _________②______________
(2)若用高锰酸钾制取氧气并用E装置收集,反应的文字表达式为____________,A装置需要改进的是_____________,实验结束时应先撤离E装置中的导管,再熄灭酒精灯,若不按此操作,将会出现的后果是___________。
(3)若欲用B和F装置制取氧气,则该反应的符号表达式为:____________,氧气应从F装置的导管口_______端通入;若欲用倒置的F装置收集氨气(NH3),则氨气应从导管口____端通入(已知氨气比空气的密度小)。
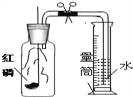
(4)下图所示装置,可用于测定空气中氧气的体积分数,集气瓶容积为250 mL,某同学在此实验中观察到量筒中减少的水的体积为50mL,则他测得的空气中氧气的体积分数为_________;在保证整个装置不漏气的前提下,如果未冷却到室温便打开弹簧夹观察量筒内减少的水的体积,则实验结果将__________(填“偏大”“偏小”或“不变”);实验完毕后,集气瓶内残余的气体主要是________(填化学符号);如果将上述实验中的红磷换成木炭,严格按操作步骤进行实验,并未发现明显的倒吸现象,其原因是________;反思此实验的探究过程,用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑___(答一条即可)。
【答案】 试管 集气瓶 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 在试管口放一团棉花 水倒吸使试管炸裂 2H2O2
锰酸钾+二氧化锰+氧气 在试管口放一团棉花 水倒吸使试管炸裂 2H2O2![]() 2H2O+O2↑ a a 20% 【答题空10】偏小 N2 木炭燃烧生成二氧化碳气体,瓶内气体体积(或压强)基本不变 生成物最好是固体(反应物不能与空气中其它成分反应等)
2H2O+O2↑ a a 20% 【答题空10】偏小 N2 木炭燃烧生成二氧化碳气体,瓶内气体体积(或压强)基本不变 生成物最好是固体(反应物不能与空气中其它成分反应等)
【解析】(1)①是试管;②是集气瓶;(2)高锰酸钾制取氧气的文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气,用高锰酸钾制取氧气,在试管口放一团棉花,以防高锰酸钾堵塞导气管。实验结束时如果先熄灭酒精灯,试管内温度降低,气体体积变小,水会倒流到试管内致使试管炸裂。(3)固液常温反应制取氧气是用过氧化氢溶液,过氧化氢
锰酸钾+二氧化锰+氧气,用高锰酸钾制取氧气,在试管口放一团棉花,以防高锰酸钾堵塞导气管。实验结束时如果先熄灭酒精灯,试管内温度降低,气体体积变小,水会倒流到试管内致使试管炸裂。(3)固液常温反应制取氧气是用过氧化氢溶液,过氧化氢![]() 水+氧气,氧气的密度比空气的密度大,占据下方空间,如果用F装置收集氧气,从导管口的a端通入。氨气的密度比空气的密度小,占据上方空间,若欲用倒置的F装置收集氨气(NH3),则氨气应从导管口a端通入。(4)集气瓶内减少的是氧气,进入的水的体积等于减少的氧气的体积,故空气中氧气的体积分数为:
水+氧气,氧气的密度比空气的密度大,占据下方空间,如果用F装置收集氧气,从导管口的a端通入。氨气的密度比空气的密度小,占据上方空间,若欲用倒置的F装置收集氨气(NH3),则氨气应从导管口a端通入。(4)集气瓶内减少的是氧气,进入的水的体积等于减少的氧气的体积,故空气中氧气的体积分数为: ![]() ×100%=20%,如果未冷却到室温,气体膨胀,体积偏大,进入的水偏少,实验结果将偏小。空气主要由氧气和氮气组成,故实验完毕后,集气瓶内残余的气体主要是N2。如果将上述实验中的红磷换成木炭,木炭燃烧生成二氧化碳气体,瓶内气体体积(或压强)基本不变,故未发现明显的倒吸现象。用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑反应物不能与空气中其它成分反应、生成物是固体。
×100%=20%,如果未冷却到室温,气体膨胀,体积偏大,进入的水偏少,实验结果将偏小。空气主要由氧气和氮气组成,故实验完毕后,集气瓶内残余的气体主要是N2。如果将上述实验中的红磷换成木炭,木炭燃烧生成二氧化碳气体,瓶内气体体积(或压强)基本不变,故未发现明显的倒吸现象。用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑反应物不能与空气中其它成分反应、生成物是固体。

【题目】实验室在进行双氧水制备氧气实验时,某同学不小心将硫酸铜溶液滴加到试管中,发现立即有大量气泡产生,该同学就此对“硫酸铜对过氧化氢溶液的分解是否也有催化作用”的课题进行研究,以下是探究的主要过程:
【提出猜想】硫酸铜可以作过氧化氢溶液的催化剂。
【实验方案】常温下取两瓶H2O2溶液,其中一瓶加入一定量的硫酸铜(另外一瓶不加),测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】如图所示为进行实验的装置图,此实验中B处宜采用的气体收集方法是____________。

【实验记录】
实验编号 | 1 | 2 |
反应物 | 6%的H2O2 | 6%的H2O2 |
反应物的量/mL | 2 | 2 |
加入物质名称 | 不加任何物质 | 1 g CuSO4 |
时间/s | 270 | 40 |
【得出结论】由该实验过程可知硫酸铜溶液对双氧水分解具有催化作用,则该实验过程发生反应的化学方程式为________________________。
【实验反思】实验结束后,小明又对硫酸铜溶液中哪种微粒对双氧水分解产生催化作用产生兴趣(该溶液中有Cu2+、SO![]() 和H2O),并进行猜想:①可能是水分子;②可能是________;③可能是Cu2+。
和H2O),并进行猜想:①可能是水分子;②可能是________;③可能是Cu2+。
小明将此猜想与同学小芳进行讨论,小芳立即否决了猜想①,原因是________________________。
【查阅资料】Na+、NO![]() 对双氧水的分解没有催化作用,据此小明在实验室里选择了两种试剂进行了实验探究,它们分别为________和________。
对双氧水的分解没有催化作用,据此小明在实验室里选择了两种试剂进行了实验探究,它们分别为________和________。