题目内容
【题目】某密闭容器中有X、氧气和二氧化碳三种物质,在一定条件下充分反应,测定反应前后各物质的质量如表,根据表中信息,判断下列说法正确的是( )
物质 | X | O2 | CO2 | H2O |
反应前质量/g | 23 | 70 | 1 | 0 |
反应后质量/g | 0 | 待测 | 45 | 27 |
A.该反应为分解反应
B.反应生成的CO2和H2O的质量比为45:27
C.表中“待测”值为48
D.X中一定含有碳、氢、氧三种元素
【答案】D
【解析】
X反应后质量减小,为反应物,二氧化碳反应后质量增加,为生成物,水反应后质量增加,为生成物。根据质量守恒定律,化学反应前后,物质的总质量不变,即:23+70+1=45+27+待测,故待测值=22,氧气反应后,质量减少,为反应物。
A、X、氧气为反应物,二氧化碳、水为生成物,该反应不符合“一变多”的特点,不属于分解反应,不符合题意;
B、反应生成的CO2和H2O的质量比为:(45-1):27=44:27,不符合题意;
C、由分析可知,表中待测值为22,不符合题意;
D、根据质量守恒定律,化学反应前后,元素的质量不变,反应后,氧元素的质量为:![]() ,故X中氧元素的质量为:56g-(70g-22g)=8g,因此X中含有氧元素,根据质量守恒定律,化学反应前后,元素的种类不变,故X中肯定含有C、H元素,符合题意。
,故X中氧元素的质量为:56g-(70g-22g)=8g,因此X中含有氧元素,根据质量守恒定律,化学反应前后,元素的种类不变,故X中肯定含有C、H元素,符合题意。
故选D。

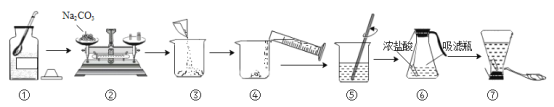
【题目】某兴趣小组利用废旧电话线中的金属铜丝进行了如下一系列实验。

①如图所示,将铜丝分别放入盛有氯化锌溶液、稀硫酸、硝酸银溶液的试管中,观察到的现象是___________,发生反应的化学方程式为:___________。
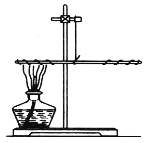
②用细线吊着的长玻璃棒的两端分别绕有40 cm长的铜丝(如图所示),使玻璃棒保持平衡,用酒精灯加热玻璃棒左端2分钟后冷却,可以观察到的现象是__________,产生该现象的原因是__________。
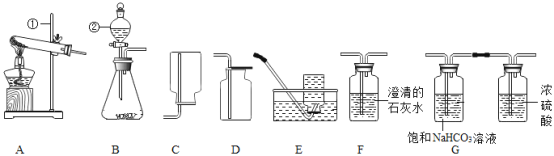
③为了研究金属铜生锈的条件,实验中将四段相同长度的铜丝分别按下图所示放置一个月,观察并记录现象如下:
E | F | G | H | |
实验装置 |
|
|
|
|
实验现象 | 铜丝不生锈 | 铜丝不生锈 | 铜丝不生锈 | 铜丝生锈 |
该实验设计体现的思想方法是_______________(选填:控制变量、对比与观察、定量分析、节能环保),结论:铜生锈是铜与 ______________作用的结果。