题目内容
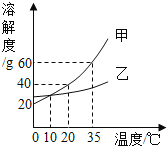
在一定量的硝酸银和硝酸铜溶液中加入锌粉,充分反应后过滤,得到滤液和滤渣,下列分析正确的是( )
A. 如果滤液显蓝色,则滤渣一定没有Cu
B. 如果滤渣只含一种金属,滤液中的溶质可能含有三种
C. 在滤渣中加入稀盐酸有气泡产生,滤液中的溶质可能含有两种
D. 在滤渣中加入稀盐酸没有气泡产生,则滤渣一定含有Ag和Cu
“84”消毒液具有漂白、杀菌、消毒的功效。在新冠肺炎预防措施中使用较为广泛。某化学兴趣小组对一瓶敞口久置的“84”消毒液的成分产生兴趣,在老师的指导下,展开探究。
(査阅资料)“84”消毒液的主要成分是次氯酸钠(NaClO)和氯化钠。NaClO为有效成分,且有腐蚀性并易与空气中的CO2反应(2NaC1O+CO2+H2O=2HC1O+Na2CO3)。NaClO溶液、HC1O都具有漂白、杀菌、消毒功效。HC1O不稳定,受热或光照条件下会发生分解生成氯化氢和氧气。
(分析讨论)小组同学经过讨论,认为该消毒液中的溶质一定有______,可能还有NaClO、Na2CO3、HClO中的一种或多种。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
I.向装入有色布条的试管中加入适量该消毒液 | 有色布条长时间不褪色 | 消毒液中不含的溶质____ |
П.另取少量该消毒液于试管中,滴入足量氯化钡溶液,静置 | 产生白色沉淀 | 消毒液中含有的溶质___ |
(交流反思)
(1)生活中“84”消毒液贮藏时应注意_____。一般不用“84”消毒液对蔬菜、水果进行消毒,其原因可能是_____。
(2)“84”消毒液与洁厕灵(主要成分是盐酸)混合使用易产生一种有毒气体,反应的化学方程式为NaClO+2HC1=NaCl+X↑+H2O,则X的化学式为______。
过氧化钠(Na2O2)是一种淡黄色固体,可用作呼吸面具中的供氧剂。某化学研究小组对过氧化钠的制备和实验室中的过氧化钠药品成分进行探究。
(查阅资料)①在点燃条件下,钠在空气中燃烧生成纯度较高的Na2O2
② 2Na2O2+2H2O = 4NaOH+O2↑ 2Na2O2+2CO2 = 2Na2CO3+O2
③金属钠遇水会发生剧烈反应生成H2
I.过氧化钠的制备
研究小组设计如图的装置进行实验室制备过氧化钠。

(1)装置B中的试剂是__。
(2)装置C中反应的化学方程式为__。
(3)装置D的作用是__。
II.开封已久的过氧化钠药品的成分测定
(定性检测)检测药品的成分。
(4)请补充完成下列实验报告中的相关内容。
实验序号 | 实验步骤 | 实验现象 | 解释或结论 |
① | 取少量固体样品于试管中,加入适量的水 | 样品全部溶解,无气泡产生 | 不含____ |
② | 取适量①中的溶液于试管中,加入过量的BaCl2溶液 | 有白色沉淀产生 | 化学方程式为___ |
③ | 待②充分静置后,向上层清液中滴入_____ | ____ | 含有氢氧化钠 |
(定量检测)检测药品的组成。
实验④:称取9.30g开封已久的过氧化钠样品于试管中,加入足量的稀硫酸,将产生的气体全部鼓入到足量的澄清石灰水中,过滤、洗涤、干燥,得到碳酸钙固体5.00g。
(5)计算确定样品中氢氧化钠的质量分数_____(写出计算过程,计算最后结果精确到0.1%)。
请根据不同的实验内容回答对应的问题。
实验内容 | 回答问题 |
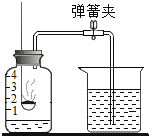
(1) 测定空气的成分 | ①该实验可得出:空气中氧气体积分数约为_____ ②写出红磷发生燃烧反应的化学方程式_____ |
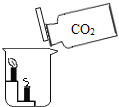
(2) 探究二氧化碳的性质 | ①该实验过程中,可观察到的现象是______ ②从实验现象得出,二氧化碳具有的性质是_____ |
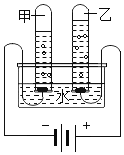
(3) 电解水 | 下列关于电解水实验的叙述正确的是_____ A 该反应是化合反应 B 正负电极上产生的气体质量之比为1:2 C 负极产生的气体能使带火星的木条复燃 D 实验说明水是由氢元素和氧元素组成的 |
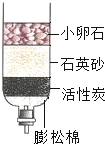
(4) 净化水 | ①实验中活性炭的作用是______ ②净化后的池塘水与矿泉水、蒸馏水、自来水四中水中属于纯净物的是____ |