题目内容
【题目】高铁酸钾(K2FeO4)是一种集吸附、凝聚、杀菌等功能为一体的新型高效水处理剂,可将水中的三氯乙烯(C2HCl3)除去85.6%,下列说法正确的是( )
A. ![]() 中三种元素的质量比是2:1:4
中三种元素的质量比是2:1:4
B. ![]() 中Fe元素的化合价为
中Fe元素的化合价为![]() 价
价
C. ![]() 中氯元素的质量分数最大
中氯元素的质量分数最大
D. ![]() 是由2个碳原子、1个氢原子和3个氯原子构成的
是由2个碳原子、1个氢原子和3个氯原子构成的
【答案】C
【解析】
A、K2FeO4中钾、铁、氧三种元素的质量比=(39×2):56:(16×4)≠2:1:4,故A错误;
B、根据化合物中各元素正负化合价的代数和为零,设:铁元素的化合价为x,则有:(+1)×2+x+(-2)×4=0,解得x=+6,故B错误;
C、C2HCl3中碳、氢、氯三种元素质量比=(12×2):1:(35.5×3)=24:1:106.5,可见其中氯元素的质量分数最大,故C正确;
D、C2HCl3是由分子构成的,不是由原子直接构成的,1个C2HCl3分子是由2个碳原子、1个氢原子和3个氯原子构成的,故D错误。故选C。

【题目】水是一种重要的物质,在日常生活和和生产实践中有着不可替代的作用。
|
|
|
|
图1 | 图2 | 图3 | 图4 |
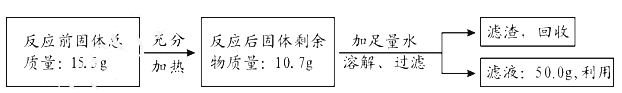
(1)水的净化
①图1所示净水器可除去水中的色素和异味,是因为其中的活性炭具有_____________性。
②在图1和图2示意的净水原理中,能降低水硬度的净水方法是图______(填“1”或2)。
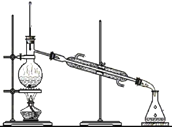
(2)水的组成。
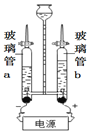
①图3是水的电解装置,接通直流电源一段时间后,玻璃管b内产生的气体是__________________,该反应的化学方程式为_____________________________。
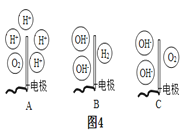
②电解水的实验中,在玻璃璃管里加含有酚酞的硫酸钠溶液,可以增强导电性。在实验过程中,观察到管a电极附近的溶液迅速变红,则该处溶液呈_______(填“酸”“碱”或“中”)性。电解后,待溶液混合均匀后测得溶液的pH=7,则图4中能表示电解时管b中水在电极端所发生变化得到的粒子是_____(填对应选项的字母)。
(3)水在化学实验中具有重要作用。
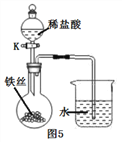
将铁丝放在潮湿的空气中(如图5所示),关闭K,一段时间后,观察到导管内液面上升;打开K,观察到导管内液面下降,导管口有气泡出。请解释导管内液面上升和下降的原因:_________________________。