题目内容
【题目】根据原子结构的知识和下图的信息填空:
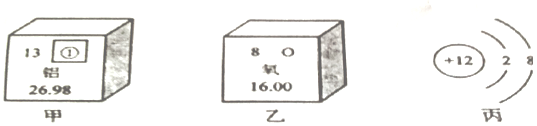
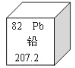
(1)甲图中①代表的元素符号是______它的离子符号是____
(2)乙图中所示元素原子的核电荷数是____丙图所示粒子属于______(填“原子”、“阳离子”或“阴离子”)。
(3)写出乙、丙两种元素的单质间发生反应生成物质的化学式为_____
【答案】Al Al3+ 8 阳离子 MgO
【解析】
(1)书写元素符号注意“一大二小”,铝的元素符号是Al.铝原子核内有13个质子,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有3个电子,在化学反应中易失去3个电子而形成带3个单位正电荷的阳离子,其离子符号为:Al3+;
(2)根据元素周期表中的一格可知,左上角的数字为8,表示原子序数为8;根据原子中原子序数=核电荷数=质子数=核外电子数,则乙图中所示元素原子的核电荷数是8;质子数=12,核外电子数=10,质子数>核外电子数,为阳离子;
(3)乙、丙两种元素的单质分别是镁和氧气,反应生成的物质是氧化镁,氧化镁中镁元素显+2价,氧元素显-2价,其化学式为:MgO。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:相等。
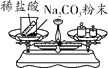
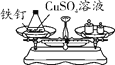
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转 |
结论 | 猜想1正确反应的化学方程式:_____ | 猜想2正确 |
(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_____中进行。
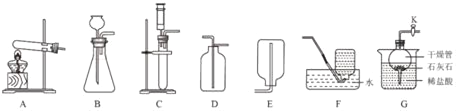
(优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是_____ (填序号),从另外两种装置中任选一种指出其不足_____。
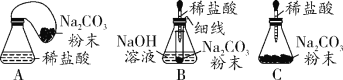
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步分析发现,反应体系中器材参加化学反应和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_______的各物质的质量总和等于反应后生成的各物质的质量总和。
(解释应用)解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_____种元素组成。
【题目】某实验小组用氯酸钾和二氧化锰混合加热制取氧气时,发现制得的气体有刺激性气味,于是对该气体成分进行探究
(提出问题)氯酸钾与氧化锰混合加热后产生的气体成分是什么?
(查阅资料)
(1)氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
(2)氯气(C12)的性质:
①有剌激性气味的气体;②溶于水;③能使湿润的淀粉碘化钾试纸变蓝。
(猜想与假设)
猜想一:该气体为O2;猜想二,该气体为Cl2;猜想三:该气体为________________________。
(实验探究)
序号 | 实验操作 | 实验现象 | 实验结论 |
1 | 小丽用排水集气法收集A、B两瓶气体,将带火星木条伸入A中,湿的淀粉碘化钾试纸伸入B中 | A中带火星木条复燃,B中淀粉碘化钾试纸不变色 | 猜想____________成立 |
2 | 小岚向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,湿润的淀粉碘化钾试纸伸入D中 | C中带火星木条复燃,D中淀粉碘化钾试纸______。 | 猜想三成立 |
(反思与评价)
小涛认为小丽的结论不正确,原因是_____________________。
(拓展应用)
实验室通常用MnO2与浓盐酸共热制取Cl2,请完成该反应的化学方程式MnO2+4HCl(浓)![]() MnCl2 +____________ +Cl2↑
MnCl2 +____________ +Cl2↑