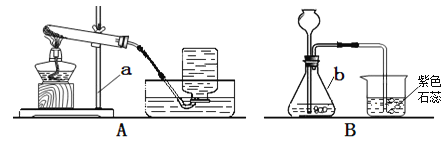
��Ŀ����
����Ŀ�����ͷ��Ǹ��ij������ɼ����ɷ�һ����NH4HCO3��NaHCO3��ijͬѧ�����ͷۼ��뵽һ�������������Ʊ�����Һ�У������������ݺͰ�ɫ���壬��Һ����ɫ��
��Ϊȷ��������弰��Һ�ijɷ֣���ͬѧ���������µ�̽����
��1��������ͨ����ɫʯ����Һ�У�ʯ����Һ����ɫ���������Ϊ ��д��ѧʽ�������ɸ�����Ļ�ѧ����ʽ�� ��
��2����ɫ�����������²²Ⲣ����ʵ�飺
���²⡿�ٰ�ɫ������CaCO3���� ���۰�ɫ������CaCO3��Ca (OH)2��
��ʵ�顿ȡϴ����İ�ɫ���壬����������ˮ�������̪�������Ա仯�����ɫ����һ���� ��
��3����������Һ��Ϊ���ݣ�
��һ���м�������ϡ���ᣬ�����壻
������һ����ͨ��������CO2�����̪�����ɰ�ɫ��������Һ�ʺ�ɫ����ԭ��Һ�������� �� ��д��ѧʽ����
��Ϊȷ�����ͷ۳ɷֺ�������ͬѧ�����˶���ʵ�飺
��4����ȡ����İ�ɫ����10 g����ּ������������ٸı�Ϊֹ���Ƶò�����������Ϊ 5.3g���ͷ���NH4HCO3��NaHCO3��������Ϊ ��
���𰸡���1��������2NH4HCO3+ Ca(OH)2 ====2 NH3��+ CaCO3��+ 2H2O��
��2����Ca(OH)2��CaCO3��
��3����Ca(OH)2��NaOH��
��4��4:21
��������
���������������ͨ����ɫʯ����Һ�У�ʯ����Һ����ɫ���������Ϊ��������Ϊ��Ӧ������NH4HCO3�����ɸ�����Ļ�ѧ����ʽ��2NH4HCO3+Ca(OH)2====2NH3��+CaCO3��+2H2O��
���²⡿�ٰ�ɫ������CaCO3����Ca(OH)2���۰�ɫ������CaCO3��Ca(OH)2��ȡϴ����İ�ɫ���壬����������ˮ�������̪�������Ա仯�����ɫ����һ����̼��ƣ���Ϊ��̪û�б�ɫ��˵��������������������������Һ��Ϊ���ݣ���һ���м�������ϡ���ᣬ�����壻˵��������̼���������һ����ͨ��������CO2�����̪�����ɰ�ɫ��������Һ�ʺ�ɫ����ԭ��Һ��������Ca(OH)2��NaOH����̼�����Ƶ�����Ϊx��
2NaHCO3![]() Na2CO3+CO2��+H2O
Na2CO3+CO2��+H2O
168 106
x 5.3g
�б���ʽ��168��X=106:5.3�ˣ�x=8.4g
���ͷ���NH4HCO3��NaHCO3��������=��10g-8.4g����8.4g=4��21