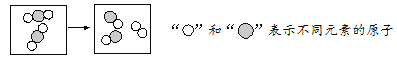题目内容
【题目】图中,甲时氧化物,其中金属元素质量分数为70%;乙是黑色粉末;丙和丁是可溶性盐。反应①和②的化学方程式分别为 、 ;试剂B是 (填化学式)溶液;反应③的发生需要氧气和水,其化学方程式 。

【答案】3CO+ Fe2O3![]() 2Fe + 3CO2 (或3C+ 2Fe2O3
2Fe + 3CO2 (或3C+ 2Fe2O3![]() 4Fe+3CO2↑等)
4Fe+3CO2↑等)
Fe2O3+6HCl = 2FeCl3 + 3H2O (或Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O等)
NaOH【或Ca(OH)2等】 4Fe(OH)2+2H2O + O2 =4 Fe(OH)3
【解析】甲是氧化物,且金属元素的含量为70%,并且还可以转化为黑色固体,说明甲是氧化铁;金属氧化物和金属同时可以与试剂A反应生成可溶性盐,根据转化关系可确定试剂A为酸,丙、丁同时与试剂B反应,生成碱,说明试剂B是一种可溶性碱。反应的化学方程式书写可根据题中提示信息来,注意质量守恒定律的应用。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目