题目内容
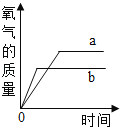
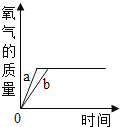
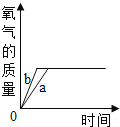
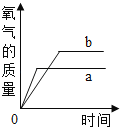
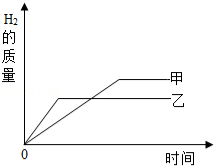
【题目】把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余.产生H2的质量随时间变化的趋势如图.下列说法正确的是( )
A.甲的活动性比乙强
B.甲的相对原子质量一定比乙小
C.反应消耗等质量的硫酸
D.反应消耗等质量的金属
【答案】D
【解析】
试题分析:等质量的甲、乙两种金属,反应后金属都没有剩余,说明酸是足量的,金属反应完全时乙用的时间少反应速度快,活动性较强,生成氢气量的不同决定了甲乙的相对原子质量的高低,利用这些知识可解决此题.
解:A、反应完全时乙用的时间少反应速度快,活动性较强,故此选项不可选.
B、金属与酸反应时,一定量金属完全反应产生氢气质量=![]() ×金属的质量,所以只有金属的质量及化合价均相同,金属的相对原子质量与反应放出氢气的多少才成反比,此图才正确,但题干没有说明两者的化合价,所以相对原子质量无法判断大小,故此选项不可选.
×金属的质量,所以只有金属的质量及化合价均相同,金属的相对原子质量与反应放出氢气的多少才成反比,此图才正确,但题干没有说明两者的化合价,所以相对原子质量无法判断大小,故此选项不可选.
C、氢气量的不同说明消耗酸的质量不同,因为氢气来源于酸中的氢,故此选项不可选.
D、放入的金属质量相等,反应后均无剩余,故此选项可选.
故选D

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目