题目内容
某兴趣小组在学习碱的化学性质时,进行了如下所示的实验.
(1)实验①中盐酸和氢氧化钠反应的化学方程式为
(2)实验②中观察到试管内有白色沉淀产生,反应的化学方程式为
(3)实验③中滴加氢氧化钠溶液后,可观察到的现象是
实验结论:碱能与多种类别的物质发生反应,包括指示剂、非金属氧化物、酸和盐类等.
【反思交流】实验结束后,同学们对实验②的废液成分进行了探究:将实验②的废液进行过滤,滤渣所含的成分是
【提出问题】滤液中所含溶质是什么物质呢?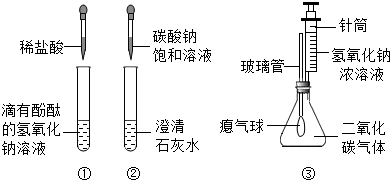
【做出猜想】猜想一:滤液中的溶质是氢氧化钠.
猜想二:滤液中的溶质是氢氧化钠和碳酸钠.
猜想三:滤液中的溶质是氢氧化钠和
【实验设计】同学们取滤液样品并加入酚酞溶液,溶液呈红色,继续逐滴加入稀盐酸,发现溶液逐渐变无色,同时有气泡产生.由此得出结论,猜想
(1)实验①中盐酸和氢氧化钠反应的化学方程式为
NaOH+HCl=NaCl+H2O
NaOH+HCl=NaCl+H2O
.(2)实验②中观察到试管内有白色沉淀产生,反应的化学方程式为
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
.(3)实验③中滴加氢氧化钠溶液后,可观察到的现象是
气球胀大
气球胀大
.实验结论:碱能与多种类别的物质发生反应,包括指示剂、非金属氧化物、酸和盐类等.
【反思交流】实验结束后,同学们对实验②的废液成分进行了探究:将实验②的废液进行过滤,滤渣所含的成分是
碳酸钙
碳酸钙
.【提出问题】滤液中所含溶质是什么物质呢?

【做出猜想】猜想一:滤液中的溶质是氢氧化钠.
猜想二:滤液中的溶质是氢氧化钠和碳酸钠.
猜想三:滤液中的溶质是氢氧化钠和
氢氧化钙
氢氧化钙
.【实验设计】同学们取滤液样品并加入酚酞溶液,溶液呈红色,继续逐滴加入稀盐酸,发现溶液逐渐变无色,同时有气泡产生.由此得出结论,猜想
二
二
正确.分析:(1)根据化学方程式书写方法来回答;(2)根据化学方程式书写方法来回答;
(3)二氧化碳与氢氧化钠反应压强减小考虑;
【反思交流】根据反应生成物来考虑;【做出猜想】根据两种反应物恰好完全反应和一方过量来进行考虑;【实验设计】根据有气泡生成,判断溶液中有碳酸钠;
(3)二氧化碳与氢氧化钠反应压强减小考虑;
【反思交流】根据反应生成物来考虑;【做出猜想】根据两种反应物恰好完全反应和一方过量来进行考虑;【实验设计】根据有气泡生成,判断溶液中有碳酸钠;
解答:解:(1)盐酸和氢氧化钠发生的是复分解反应相互交换成分,生成氯化钠和水,反应的化学方程式为:NaOH+HCl=NaCl+H2O;
(2)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(3)二氧化碳与氢氧化钠反应压强减小,在外界大气压的作用下空气进入气球,气球胀大;
(4)①由于盐酸与氢氧化钠反应生成了氯化钠,而氯化钠显中性又不易和其它物质反应,所以一定含有氯化钠;
②使废液呈碱性的物质有氢氧化钠、氢氧化钙、碳酸钠,溶液中不能剩氢氧化钙和碳酸钠,因为二者继续反应,所以只有还有可能是氢氧化钠和氢氧化钙了;
【反思交流】将实验②是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故将其废液进行过滤,滤渣所含的成分是碳酸钙.
【做出猜想】如果碳酸钠和氢氧化钙恰好完全反应,则溶质只有氢氧化钠,也就是猜想一;
如果碳酸钠过量,则溶质为氢氧化钠和碳酸钠,也就是猜想二;
如果氢氧化钙过量,则溶质为氢氧化钠和氢氧化钙,也就是猜想三;
【实验设计】取滤液样品并加入酚酞溶液,溶液呈红色,继续逐滴加入稀盐酸,发现溶液逐渐变无色,同时有气泡产生,气泡为盐酸与碳酸钠反应生成的二氧化碳气体,故证明猜想二正确;
(1)NaOH+HCl=NaCl+H2O;(2)Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(3)气球胀大【反思交流】碳酸钙;【做出猜想】氢氧化钙;【实验设计】二;
(2)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(3)二氧化碳与氢氧化钠反应压强减小,在外界大气压的作用下空气进入气球,气球胀大;
(4)①由于盐酸与氢氧化钠反应生成了氯化钠,而氯化钠显中性又不易和其它物质反应,所以一定含有氯化钠;
②使废液呈碱性的物质有氢氧化钠、氢氧化钙、碳酸钠,溶液中不能剩氢氧化钙和碳酸钠,因为二者继续反应,所以只有还有可能是氢氧化钠和氢氧化钙了;
【反思交流】将实验②是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,故将其废液进行过滤,滤渣所含的成分是碳酸钙.
【做出猜想】如果碳酸钠和氢氧化钙恰好完全反应,则溶质只有氢氧化钠,也就是猜想一;
如果碳酸钠过量,则溶质为氢氧化钠和碳酸钠,也就是猜想二;
如果氢氧化钙过量,则溶质为氢氧化钠和氢氧化钙,也就是猜想三;
【实验设计】取滤液样品并加入酚酞溶液,溶液呈红色,继续逐滴加入稀盐酸,发现溶液逐渐变无色,同时有气泡产生,气泡为盐酸与碳酸钠反应生成的二氧化碳气体,故证明猜想二正确;
(1)NaOH+HCl=NaCl+H2O;(2)Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(3)气球胀大【反思交流】碳酸钙;【做出猜想】氢氧化钙;【实验设计】二;
点评:通过回答本题知道了碳酸根的检验方法,掌握了在分析化学反应后所得物质的成分时不仅考虑生成物有什么,还需要考虑反应物中什么物质过量问题.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目


