题目内容
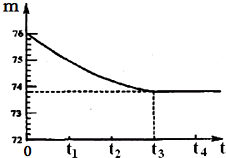
小琳取了一块石灰石(杂质既不溶于水也不与盐酸反应).将其敲打粉碎后,称出一定质量的样品放入烧杯内,然后加入50g稀盐酸,恰好完全反应.反应所需时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示.(烧杯质量为18g).
试计算:
(1)生成二氧化碳有______g.
(2)石灰石的纯度.
(3)反应后溶液中溶质质量分数.
试计算:
(1)生成二氧化碳有______g.
(2)石灰石的纯度.
(3)反应后溶液中溶质质量分数.

(1)图中质量轴上每个小刻度表示0.2g,所以完全放出气体后剩余物质总质量为73.8g;
由质量守恒定律,因此放出气体二氧化碳的质量=76g-73.8g=2.2g;故填:2.2;
(2)设石灰石样品中碳酸钙的质量为x,生成氯化钙的质量为y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100111 44
xy 2.2g
=
解得:x=5g
=
y=5.55g
石灰石样品的质量=76g-50g-18g=8g
石灰石样品中碳酸钙的质量分数=
×100%=62.5%
(3)反应后溶液中溶质质量分数=
×100%=10.5%
答:(2)该石灰石样品中碳酸钙的质量分数是62.5%;(3)反应后溶液中溶质质量分数为10.5%.
由质量守恒定律,因此放出气体二氧化碳的质量=76g-73.8g=2.2g;故填:2.2;
(2)设石灰石样品中碳酸钙的质量为x,生成氯化钙的质量为y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100111 44
xy 2.2g
| 100 |
| x |
| 44 |
| 2.2g |
解得:x=5g
| 111 |
| y |
| 44 |
| 2.2g |
y=5.55g
石灰石样品的质量=76g-50g-18g=8g
石灰石样品中碳酸钙的质量分数=
| 5g |
| 8g |
(3)反应后溶液中溶质质量分数=
| 5.55g |
| 5g+50g-2.2g |
答:(2)该石灰石样品中碳酸钙的质量分数是62.5%;(3)反应后溶液中溶质质量分数为10.5%.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目

