题目内容
【题目】金属材料用途广泛,根据所学知识回答:
(1)我国科技迅猛发展,航海及军事领域取得重大突破。建造航母用到了钛合金,工业制钛有一种反应为:![]() ,X的化学式为_____,钛合金具有强度高、硬度大、质量轻、耐腐蚀等性能。
,X的化学式为_____,钛合金具有强度高、硬度大、质量轻、耐腐蚀等性能。
(2)航母外壳使用的是钢铁材料并用涂料将钢铁材料覆盖,使用涂料是为了防止钢铁材料与_____接触而锈蚀。
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是_____(填序号)。
A ![]() 溶液中加入足置铜粉后,再加入铁粉
溶液中加入足置铜粉后,再加入铁粉
B ![]() 溶液中加入足量铁粉后,再加入
溶液中加入足量铁粉后,再加入![]() 溶液
溶液
(4)冶炼2900t含四氧化三铁80%的磁铁矿石,理论上能得到含杂质2%的生铁的质量是_____t(结果精确到0.1)。
【答案】![]() 水和氧气 B 1714.3
水和氧气 B 1714.3
【解析】
(1)由化学方程式:![]() 可得,反应物中包含1个Ti原子,4个F原子,4个H原子,2个S原子,8个O原子,生成物中包含4个H原子,4个F原子,1个Ti原子,2个O原子,所以2X中包含2个S原子,6个O原子,即X的化学式为SO3;
可得,反应物中包含1个Ti原子,4个F原子,4个H原子,2个S原子,8个O原子,生成物中包含4个H原子,4个F原子,1个Ti原子,2个O原子,所以2X中包含2个S原子,6个O原子,即X的化学式为SO3;
(2)钢铁材料与空气中的水和氧气接触易生锈,使用涂料是为了防止钢铁材料与氧气和水接触;
(3)
A、![]() 溶液中加入足量铜粉,不会发生反应,说明Zn的活动性比铜强;再加入铁粉,也不会发生反应,说明Zn的活动性比铁强,不能证明铜和铁的顺序,故不能探究三种金属的活动顺序;
溶液中加入足量铜粉,不会发生反应,说明Zn的活动性比铜强;再加入铁粉,也不会发生反应,说明Zn的活动性比铁强,不能证明铜和铁的顺序,故不能探究三种金属的活动顺序;
B、![]() 溶液中加入足量铁粉,不会发生反应,说明Zn的活动性比铁强;再加入
溶液中加入足量铁粉,不会发生反应,说明Zn的活动性比铁强;再加入![]() 溶液,会与铁粉反应生成铜单质和氯化亚铁,说明铁的金属性比铜强,所以三种金属的活动性顺序为Zn>Fe大于Cu,故选B;
溶液,会与铁粉反应生成铜单质和氯化亚铁,说明铁的金属性比铜强,所以三种金属的活动性顺序为Zn>Fe大于Cu,故选B;
(4)可以用CO于Fe3O4在高温下反应冶炼铁,设能得到含杂质2%的生铁的质量是x
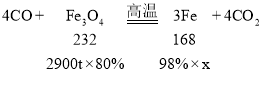
x≈1714.3t

【题目】Na2CO3和NaHCO3有很多相似的化学性质,例如它们都能与稀盐酸反应生成_____气体。某学习小组对它们的鉴别方法产生了探究兴趣。
(提出问题)如何鉴别Na2CO3和NaHCO3呢?
(查阅资料)(1)NaHCO3固体受热分解生成碳酸钠和两种氧化物。
(2)Ca(HCO3)2可溶于水。
(3)通常状况下,NaHCO3是一种白色晶体,溶解度小于Na2CO3的溶解度,饱和的Na2CO3溶液中通入CO2气体,可生成NaHCO3。
(作出猜想)猜想一:可用酚酞溶液鉴别Na2CO3和NaHCO3溶液。
猜想二:可用加热的方法鉴别Na2CO3和NaHCO3固体。
猜想三:可用澄清石灰水鉴别Na2CO3和NaHCO3溶液。
猜想四:可用CO2气体鉴别Na2CO3和NaHCO3溶液。
小组同学一致认为猜想一不正确,理由是_____。
(实验探究)请你与小组同学一起探究。
实验操作 | 实验现象 | 实验结论 | |
实验1 | 分别取少量的Na2CO3和NaHCO3 固体于试管中加热,并将产生的气体通入澄清石灰水 | 加热Na2CO3时,澄清石灰水无变化;加热NaHCO3时,澄清石灰水变浑浊 | _____ |
实验2 | 分别取少量Na2CO3和NaHCO3溶液于试管中,加入澄清石灰水 | 两支试管中均产生了白色沉淀 | 猜想三 不正确 |
实验3 | 往盛有饱和Na2CO3和NaHCO3溶液的两支试管中分别通入足量的CO2气体 | 观察到_____ | 猜想四 正确 |
(问题讨论)
同学们对实验2的实验现象进行分析。从物质在溶液中解离出不同离子的微观角度分析,Na2CO3溶液与澄清石灰水发生反应的本质原因是_____,该反应的基本类型是_____。石灰水与NaHCO3溶液也能反应生成白色沉淀,老师指出其反应原理较复杂,有待于今后学习中进一步探究。
(拓展应用)
除去固体Na2CO3中混有的少量NaHCO3,可用的方法是_____(用化学方程式表示)。
【题目】下列除去杂质所选用的试剂正确的是( )
选项 | 物质 | 杂质(少量) | 除杂试剂 |
A | N2 | O2 | 灼热的铜网 |
B | CaO | Ca(OH)2 | 水 |
C | NaCl溶液 | Na2SO4 | Ba(NO3)2溶液 |
D | FeSO4溶液 | CuSO4 | 锌粉 |
A. AB. BC. CD. D