题目内容
 人类生活离不开金属.铁是生活中常用的金属.下图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
人类生活离不开金属.铁是生活中常用的金属.下图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热. ①发热剂需接触到空气才会发热,原因是铁要与
水
水
、氧气
氧气
等物质共同作用才会生锈.②推测发热剂成分中氯化钠的作用是
加速铁粉生锈,更快地放出热量
加速铁粉生锈,更快地放出热量
.③要防止家里常用的菜刀生锈,通常采用的方法是
保持表面的清洁与干燥
保持表面的清洁与干燥
;④金属矿物的储量有限,而且不能再生;目前世界上已有50%以上的废钢铁得到回收利用,其目的是
节约金属资源
节约金属资源
(填“合理开采矿物”或“节约金属资源”).分析:①②从铁生锈的条件考虑,铁只有与水、空气同时接触时才生锈,如果有盐溶液存在时,会使生锈速度加快.
③根据防止金属锈蚀的方法分析;
④废钢铁得到回收利用的意义有:节约金属资源、减少对环境的污染、节约能源、实现了对资源的循环利用等.
③根据防止金属锈蚀的方法分析;
④废钢铁得到回收利用的意义有:节约金属资源、减少对环境的污染、节约能源、实现了对资源的循环利用等.
解答:解:①②铁要与水、氧气同时接触才能生锈,缺一不可,当有盐溶液存在时,生锈的速度加快,所以发热剂成分中有氯化钠.
故答案为:①水、氧气;②加速铁粉生锈,更快地放出热量;
③要防止家里常用的菜刀生锈,通常采用的方法是保持表面的清洁与干燥.
故答案为:保持表面的清洁与干燥;
④废钢铁得到回收利用的意义有:节约金属资源、减少对环境的污染、节约能源、实现了对资源的循环利用等.
故答案为:节约金属资源.
故答案为:①水、氧气;②加速铁粉生锈,更快地放出热量;
③要防止家里常用的菜刀生锈,通常采用的方法是保持表面的清洁与干燥.
故答案为:保持表面的清洁与干燥;
④废钢铁得到回收利用的意义有:节约金属资源、减少对环境的污染、节约能源、实现了对资源的循环利用等.
故答案为:节约金属资源.
点评:本考点了金属的锈蚀条件及其防护,属于结合课本知识的信息.要知道金属锈蚀的条件和防止金属制品生锈的措施,并结合生活实际,选择比较好防止金属生锈的措施和保护金属资源的方法,并知道金属回收的重要意义.

练习册系列答案
相关题目
人类生活离不开金属.
(1)生活中应用铁锅炒菜,主要是运用了铁具有 性(填“导热”或“延展”).
(2)如图是某“取暖片”的图片.该“取暖片”的发热过程是利用铁生锈的原理,铁生锈是铁与水和 共同作用的结果.

(3)应用金属活动性顺序能帮助我们进一步学习金属的性质.已知下列每组物质均能发生置换反应.
A.Fe和CuSO4溶液B.Mn和FeSO4溶液
①写出Mn和FeSO4溶液反应的化学方程式(Mn在生成物中显+2价) .
②由上述信息得出Fe、Cu、Mn三种金属的活动性由强到弱的顺序为 .
(4)为了测定黄铜屑(锌铜合金)中锌的质量分数,同学们进行了以下实验:取20g黄铜屑放入锥形瓶中,再加入足量的稀硫酸,观察到不同时刻天平的读数如下表所示:
请计算反应生成氢气的总质量为 g,黄铜屑中锌的质量分数为 .
(1)生活中应用铁锅炒菜,主要是运用了铁具有
(2)如图是某“取暖片”的图片.该“取暖片”的发热过程是利用铁生锈的原理,铁生锈是铁与水和

(3)应用金属活动性顺序能帮助我们进一步学习金属的性质.已知下列每组物质均能发生置换反应.
A.Fe和CuSO4溶液B.Mn和FeSO4溶液
①写出Mn和FeSO4溶液反应的化学方程式(Mn在生成物中显+2价)
②由上述信息得出Fe、Cu、Mn三种金属的活动性由强到弱的顺序为
(4)为了测定黄铜屑(锌铜合金)中锌的质量分数,同学们进行了以下实验:取20g黄铜屑放入锥形瓶中,再加入足量的稀硫酸,观察到不同时刻天平的读数如下表所示:
| 反应时间/min | 0 | 1 | 2 | 3 | 4 |
| 锥形瓶及所盛物质总质量/g | 220.70 | 220.44 | 220.34 | 220.30 | 220.30 |
 (2012?通州区二模)人类生活离不开金属.
(2012?通州区二模)人类生活离不开金属.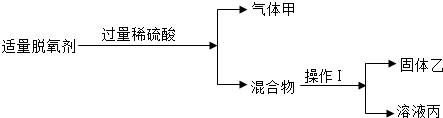
 人类生活离不开金属.铁是生活中常用的金属.右图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
人类生活离不开金属.铁是生活中常用的金属.右图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.