题目内容
【题目】请结合下图回答问题:
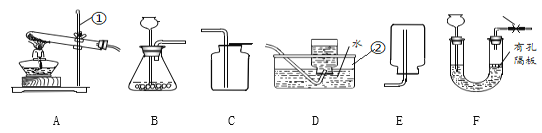
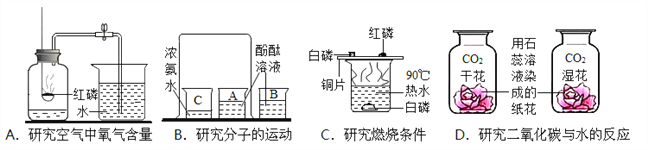
(1)标号①②的仪器名称:①________,②________.
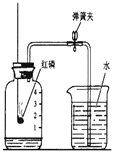
(2)实验室加热高锰酸钾选用A、D装置制取O2,实验过程中当观察到_______(填写现象)时,说明气体集满,接下来应先_____(填“从水中取出导气管”或“熄灭酒精灯”).若发现D中的水变红,可能原因是_________
(3)实验室可用(NH4)2SO4固体和熟石灰混合加热制取NH3,应选择发生装置为____(选填序号,下同).NH3是一种密度小于空气,极易溶于水的气体,则可用____收集.
(4)选择发生装置B和收集装置____可以用于实验室制取CO2,写出该反应的化学式表达式______,检验CO2是否收集满的方法是______,若将发生装置由B改为F,其优点是______.
(5)在用KClO3加热制O2的过程中,发现产生O2的反应速率很慢,经检查不是KClO3变质,也不是装置气密性不好,你认为最可能的原因是________.
【答案】铁架台 水槽 集气瓶口有大气泡 从水中取出导气管 试管口没有放棉花团(答案合理给分) A E C CaCO3+HCl![]() CaCl2+H2O+CO2 将燃着的木条放在集气瓶口,若木条熄灭,则已满 控制反应的发生和停止(答案合理给分) 没有加催化剂(如二氧化锰)
CaCl2+H2O+CO2 将燃着的木条放在集气瓶口,若木条熄灭,则已满 控制反应的发生和停止(答案合理给分) 没有加催化剂(如二氧化锰)
【解析】
(1)仪器①是铁架台,②是水槽;故填:铁架台;水槽;
(2)加热高锰酸钾制取氧气,并用排水法收集时,集气瓶口有大气泡向外冒出时,说明氧气已满;先将导管移出水面,然后再熄灭酒精灯,以防冷水倒吸、炸裂试管;若发现D中的水变红,可能原因是试管口没有放棉花团,高锰酸钾颗粒进入导气管,造成水槽中的水变红;
(3)实验室可用(NH4)2SO4固体和熟石灰混合加热制取NH3,属于固体加热型,选择装置A来制取;NH3是一种密度小于空气,极易溶于水的气体,则可用向下排空气法来收集,收集装置选E;
(4)二氧化碳能溶于水,密度比空气大,可用向上排空气法来收集,收集装置选C;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学式表达式CaCO3+HCl![]() CaCl2+H2O+CO2;二氧化碳不燃烧、也不支持燃烧,CO2验满方法是将燃着的木条放在集气瓶口,若木条熄灭,则已满;在装置F中,固体药品物放在多孔隔板上,稀盐酸从长颈漏斗中加入。关闭开关时,U型管右端的气体增多,压强增大,液面下降,固体和液体分离,反应停止,打开开关时,气体导出,U型管右端的气体减少,压强减小,液面上升,液体和固体混合,反应进行。
CaCl2+H2O+CO2;二氧化碳不燃烧、也不支持燃烧,CO2验满方法是将燃着的木条放在集气瓶口,若木条熄灭,则已满;在装置F中,固体药品物放在多孔隔板上,稀盐酸从长颈漏斗中加入。关闭开关时,U型管右端的气体增多,压强增大,液面下降,固体和液体分离,反应停止,打开开关时,气体导出,U型管右端的气体减少,压强减小,液面上升,液体和固体混合,反应进行。
若将发生装置由B改为F,其优点是可以控制反应的开始与停止;
(5)在用KClO3加热制O2的过程中,发现产生O2的反应速率很慢,经检查不是KClO3变质,也不是装置气密性不好,催化剂可以加快反应速率,最可能的原因是没有加催化剂(如二氧化锰)。

 阅读快车系列答案
阅读快车系列答案【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验:
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ、将3g氯酸钾与1g二氧化锰均匀混合加热
Ⅱ、将xg氯酸钾与1g氧化铜均匀混合加热
在相同温度下,比较两组实验产生氧气的快慢。
Ⅰ反应中文字表达式是____________
Ⅱ中x的值应为______
②乙探究了影响过氧化氢分解速度的某种因素。实验数据记录如下:
过氧化氢的质量 | 过氧化氢的浓度 | 二氧化锰的质量 | 相同时间内产生氧气的体积 | |
Ⅰ | 50g | 1% | 0.1g | 9mL |
Ⅱ | 50g | 2% | 0.1g | 16mL |
Ⅲ | 50g | 4% | 0.1g | 31mL |
本实验中,测量氧气体积的装置是____________(填编号)
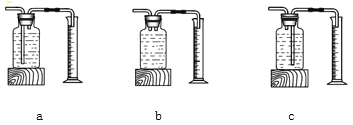
实验结论如下:在相同条件下,_______,过氧化氢分解得越快。