题目内容
通过学习,我们知道:沼气的主要成分是甲烷。那么沼气池中除了甲烷以外还有什么气体呢?带着这个疑问,我们学习小组的同学进行了以下探究活动。
【查阅资料】①沼气池中除了有甲烷外,还可能有CO、CO2、H2S等。
②H2S气体有毒,能燃烧,能与CuSO4溶液反应生成黑色CuS沉淀。
【收集气体】将不加盖的矿泉水瓶装满水,用细绳吊入池中,使瓶中的水全部倒出,然后迅速拉起矿泉水瓶,盖上瓶盖。这种方法属于 集气法。
【提出猜想】小组的同学对沼气含有上述气体中最少3种成分的猜想如下:
小吴的猜想:有CH 4、CO、H2S
4、CO、H2S
小周的猜想:有CH4、CO2、H2S
小施的猜想:有CH4、CO 、CO2
我的猜想:有 。
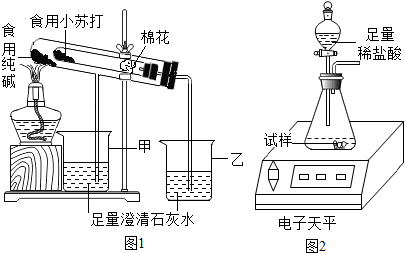
 【实验方案】小组的同学在老师的指导下,共同设计了下图的装置并进行探究(除B外其它每步反应或作用都是完全的)
【实验方案】小组的同学在老师的指导下,共同设计了下图的装置并进行探究(除B外其它每步反应或作用都是完全的)
【实验过程】
| E装置总质量 | F装置总质量 | |
| 反应前 | 156.6g | 156.8g |
| 反应后 | 158.4g | 159.0g |
(1)A、B装置中都产生明显的现象,则沼气中肯定含 气体,A中变化的
化学方程式为 ,
B中变化的现象为 ;
(2)装置C的作用是 ;
(3)装置D中的药品是 ;
(4)实验过程中记录的实验数据如右表
【实验结论】 同学的猜想正确。
【拓展应用】沼气池的残余物可作农家肥,在清理沼气池中的残余物时,从安全的角度考虑应注意的事项: (答一点)。
【收集气体】排水
【提出猜想】CH4、CO 、CO2、H2S(气体的排列顺序不限)
【实验过程】(1)H2S 、CO2 H2S + CuSO4 =Cu S↓ + H2SO4 生成白色沉淀。
(2)完全除去CO2,排除干扰。
(3)浓硫酸。
【实验结论】小周
【拓展应用】严禁烟火、戴防毒面具等(只答一点即可,合理的答案均给分)

 通过学习,我们知道有多种途径可以制取氧气.如:
通过学习,我们知道有多种途径可以制取氧气.如: