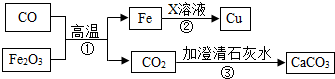
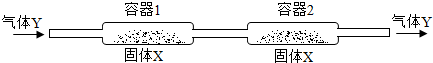
��Ŀ����
��2013?������һģ��ij��ȤС���ʳ�ô����ʳ��С�մ����ַ�ĩ��������̽����
��һ��������̽����
[��������]
[ʵ��̽��]
��1��̽������ˮ��Һ����ԵIJ���
С���ֱ����Ũ�ȵ�������Һ�е����̪��Һ���������߶���
��2����֤���ַ�ĩ���ȶ���
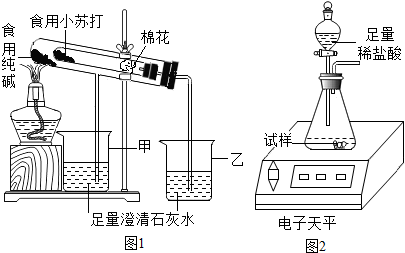
����ʦ��ָ���£���С�鰴ͼ1װ�ý���ʵ��������۲쵽
����չ���졿
��3��ͨ��ѧϰ������֪��С�մ�NaHCO3��������ʳƷ��ҵ�⣬���ճ����ʵ�����л��кܶ�Ӧ�ã��Ծ�һ����
������������̽����
��4��ȡʳ�ô����ĩ����������ͼ2װ�ý���ʵ��ⶨ�����ݼ�¼���£�
�ٷ�Ӧ����CO2������Ϊ
��ͨ������ȷ��ʳ�ô����ĩ��Na2CO3����������Ϊ
�������õĽ����ʵ�ʴ��ȸߣ����ܵ�ԭ����
��һ��������̽����
[��������]
| ���� | ʳ�ô��� | ʳ��С�մ� |
| ��Ҫ�ɷ� | Na2CO3 | NaHCO3 |
| ����� | ˮ��Һ�Լ��� | ˮ��Һ�Լ��� |
| ���ȶ��� | ���Ȳ��ֽ� | 270��ʱ��ȫ�ֽ�Ϊ̼���ơ�������̼��ˮ |
��1��̽������ˮ��Һ����ԵIJ���
С���ֱ����Ũ�ȵ�������Һ�е����̪��Һ���������߶���
��
��
ɫ����ʳ�ô�����Һ����ɫ����ɴ��Ʋ����ʳ�ô���
ʳ�ô���
��Һ���Ը�ǿ��С����ΪҪ�Ƚ�������Һ�ļ���ǿ������ֱ����pH��ֽ
pH��ֽ
���вⶨ����2����֤���ַ�ĩ���ȶ���

����ʦ��ָ���£���С�鰴ͼ1װ�ý���ʵ��������۲쵽
��
��
����ס����ҡ����ձ��г���ʯ��ˮ����ǣ��Թ��з�����Ӧ�Ļ�ѧ����ʽΪ2NaHCO3
Na2CO3+CO2��+H2O
| ||
2NaHCO3
Na2CO3+CO2��+H2O
��װ��������������
| ||
��ֹ����ʱС�մ�NaHCO3����ĩ���뵼��
��ֹ����ʱС�մ�NaHCO3����ĩ���뵼��
������չ���졿
��3��ͨ��ѧϰ������֪��С�մ�NaHCO3��������ʳƷ��ҵ�⣬���ճ����ʵ�����л��кܶ�Ӧ�ã��Ծ�һ����
��������
��������
��������������̽����
��4��ȡʳ�ô����ĩ����������ͼ2װ�ý���ʵ��ⶨ�����ݼ�¼���£�
| ������Ŀ | ����ʱ�� | ����/g |
| ���� | 11.0 | |
| װ��+ϡ���� | 160.0 | |
| װ��+ϡ����+���� | ��Ӧ��ʼ��20s | 167.0 |
| װ��+ϡ����+���� | ��Ӧ��ʼ��30s | 166.6 |
| װ��+ϡ����+���� | ��Ӧ��ʼ��90s | 166.6 |
4.4
4.4
g����ͨ������ȷ��ʳ�ô����ĩ��Na2CO3����������Ϊ
96.4
96.4
%���������һλС�����������õĽ����ʵ�ʴ��ȸߣ����ܵ�ԭ����
ϡ����ӷ�����HCl���壨��ˮ��������CO2�����ų����������ⴿ��ƫ��
ϡ����ӷ�����HCl���壨��ˮ��������CO2�����ų����������ⴿ��ƫ��
������һ�ּ��ɣ��������������е�֪ʶ���з�������̪��Һ�ڼ�����Һ��Ϊ��ɫ��������Һ��pHԽ����Խǿ��̼�������ڼ���ʱ�ֽܷ�����̼���ơ�ˮ�Ͷ�����̼������̼���������ᷴӦ�������仯������������ɶ�����̼�������Լ�����̼���Ƶ������������ݴ˽�ɣ�
����⣺��1��ʳ�ô����Լ�̼�����Ƶ�ˮ��Һ���ʼ��ԣ���ʹ��̪��Һ��죬ʳ�ô�����Һ����ɫ���˵������ļ��Ա�̼�����Ƶļ���Ҫǿ���ⶨ��Һ��pH����ʹ��pH��ֽ������죬ʳ�ô��pH��ֽ��
��2��̼�����������ֽܷ�����̼���ơ�ˮ�Ͷ�����̼����̼�������Ȳ��ֽ⣬�����ձ��е�ʯ��ˮ�����ǣ����Թܿڷ�һ�����ܷ�ֹ����̼������ʱ���ĩ���������е��ܣ�����ң�2NaHCO3
Na2CO3+CO2��+H2O����ֹ����ʱС�մ��ĩ���뵼�ܣ�
��3��̼�������������ᷴӦ��������������θ����࣬�������θ����ࣻ
��4�������ɶ�����̼������Ϊ��11.0g+160g-166.6g=4.4g�����4.4��
��������4.4g������̼��Ҫ̼���Ƶ�����Ϊx
Na2CO3+2HCl=2NaCl+H2O+CO2��
106 44
x 4.4g
=
x=10.6g
ʳ�ô����ĩ��Na2CO3����������Ϊ��
��100%��96.4%
���96.4��
��������Ľ��ƫ��������Dz����Ķ�����̼�л����������ʱ���ˮ����������ӷ������Ȼ��⣬���¶�����̼������ƫ�Ӷ������̼���Ƶ�����ƫ���ԭ���ϡ����ӷ�����HCl���壨��ˮ��������CO2�����ų����������ⴿ��ƫ��
��2��̼�����������ֽܷ�����̼���ơ�ˮ�Ͷ�����̼����̼�������Ȳ��ֽ⣬�����ձ��е�ʯ��ˮ�����ǣ����Թܿڷ�һ�����ܷ�ֹ����̼������ʱ���ĩ���������е��ܣ�����ң�2NaHCO3
| ||
��3��̼�������������ᷴӦ��������������θ����࣬�������θ����ࣻ
��4�������ɶ�����̼������Ϊ��11.0g+160g-166.6g=4.4g�����4.4��
��������4.4g������̼��Ҫ̼���Ƶ�����Ϊx
Na2CO3+2HCl=2NaCl+H2O+CO2��
106 44
x 4.4g
| 106 |
| x |
| 44 |
| 4.4g |
ʳ�ô����ĩ��Na2CO3����������Ϊ��
| 10.6g |
| 11.0g |
���96.4��
��������Ľ��ƫ��������Dz����Ķ�����̼�л����������ʱ���ˮ����������ӷ������Ȼ��⣬���¶�����̼������ƫ�Ӷ������̼���Ƶ�����ƫ���ԭ���ϡ����ӷ�����HCl���壨��ˮ��������CO2�����ų����������ⴿ��ƫ��
���������⿼����̼���Ƶ������Լ��йصļ��㣬��ɴ��⣬�����������е�֪ʶ���У�

��ϰ��ϵ�д�
 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
�����Ŀ