题目内容
【题目】A~G是初中化学常见的物质,它们之间的转化关系如下图所示。已知:A在常温下是一种无色液体,D是天然气的主要成分,G是一种重要的建筑材料的主要成分,E是一种金属氧化物,E与A反应放出大量的热。请回答下列问题:
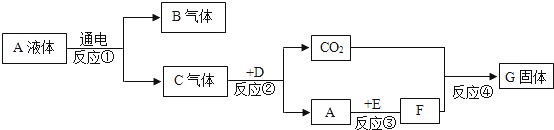
(1)写出E物质的化学式_______。
(2)写出下列反应的化学方程式:②_______;④_______。
(3)E在日常生活中用途广泛,请写出其中一点_______。
(4)B是最清洁的燃料,但是作为燃料暂时还不能泛使用,你认为原因是_______(请写出其中的一种)。
【答案】CaO ![]()
![]() 作干燥剂(合理即可,如自热火锅发热剂等) 制取成本高(或贮存困难)。
作干燥剂(合理即可,如自热火锅发热剂等) 制取成本高(或贮存困难)。
【解析】
D是天然气的主要成分,说明D是甲烷,G是一种重要建筑材料的主要成分,说明G是碳酸钙,E是一种金属氧化物,与A反应能生成一种常见的碱,而A在常温下是一种无色液体,说明E是氧化钙,A为水,那么B和C为氢气和氧气,C和D反应生成二氧化碳和A即水,说明C为氧气,而B为氢气,水和E反应生成了F,说明F为氢氧化钙,氢氧化钙和二氧化碳反应生成了碳酸钙。
(1)由分析知E是氧化钙,化学式为:CaO;
(2)C是氧气D是甲烷,故②的反应方程式为:![]() ;反应④是二氧化碳和氢氧化钙的反应方程式为:
;反应④是二氧化碳和氢氧化钙的反应方程式为:![]() ;
;
(3)E是氧化钙,极易与水结合生成氧化钙,在日常生活中常被用作干燥剂;
(4)B为氢气在燃烧时产生水,不会污染空气,等质量的可燃物,氢气的热值高,同时用水即可制得,所以来源比较广泛,但是由于它是气体,液化需要的条件比较苛刻,且制取成本较高,所以难以推广使用。

【题目】“舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的舞台。大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒中的乙醇生成乙酸乙酯。下表中是几种常见的酯,请完成下列问题:
酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
化学式 | C2H4O2 | C3H6O2 | C3H6O2 | X |
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为 _______;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为_______(计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X的化学式为________。
【题目】某同学用如图装置,进行有关碳及其氧化物的实验(图中夹持已略去),在完成气密性检查后加入药品,并已在装置中充满二氧化碳。
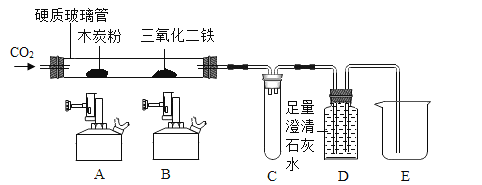
实验步骤 | 实验现象 | 实验分析 |
①缓缓通入CO2,点燃A处木炭粉减少。D中有气泡产生 | 酒精喷灯,加热一段时间澄清石灰水变浑浊且_________ | 硬质玻璃管中发生反应的化学方程式为:______。 |
②点燃B处酒精喷灯,加热一段时间 | B处玻璃管内______ | 实验①②说明______有还原性 |
③停止通入二氧化碳,熄灭A、B两处的火焰 | D中液体沿导管进入C中 | 出现此现象的原因是______ |
(2)有同学认为该装置需要添加尾气处理装置,你认为是否需要并说明理由______。
【题目】某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。
(设计实验)用一氧化碳还原纯净的氧化铁粉末,实验装置如下图。

(进行实验)该小组按上述实验设计,在一定温度下进行了实验。实验开始时,先向装置通一会儿一氧化碳,然后再加热,目的是_________。
实验过程中测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
(分析与讨论)
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
(查阅资料)
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关。
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁。
物质性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
颜色 | 黑色 | 黑色 | 红色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
(实验与猜想)
(1)该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和 ____________。
(2)进行猜想:黑色固体粉末可能有三种:
a.全部为铁 b.全部为四氧化三铁c._________。
(3)通过实验中获得的数据进行计算,得出结论:猜想 _________。
(填“a”“b”或“c”)正确.
(4)实验装置图中采用虚线框内的装置,其作用有 ___________。
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.