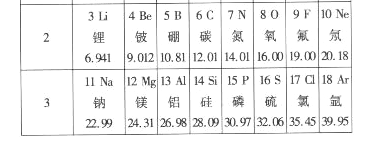
题目内容
【题目】A,B,C三种固体物质的溶解度曲线如图,请回答下列问题: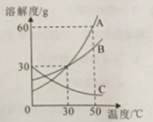
(1)随着温度升高,C的溶解度(填“增大”“减小”或“不变”),温度为℃时,A,B的溶解度相等。
(2)30℃时,将35gB放入100g水中,充分溶解后所得的溶液是(填“饱和”或“不饱和”)溶液。
(3)将30℃时A的饱和溶液升温到50℃,其溶质的质量分数(填“增大”“减小”或“不变”)。
(4)50℃时,A,B,C三种物质的溶解度由大到小的顺序是。
(5)若A的饱和溶液中含有物质C,提纯A的方法是。
【答案】
(1)减小,30
(2)饱和
(3)不变
(4)A>B>C
(5)降温结晶
【解析】解:(1)从图中我们可以看出随着温度升高,C的溶解度减小,在30℃时,A、B相交,溶解度相等;(2)30℃时B的溶解度为30g,含有就是30℃时,100g水中最多溶解30gB,将35gB放入100g水中只能溶解30g,形成的溶液是饱和溶液;(3)A的溶解度随温度的升高而增大,30℃时A的饱和溶液升温到50℃由饱和溶液变为不饱和溶液,溶质质量和溶液质量都没变,所以溶质质量分数也就没变;(4)50℃时,A,B,C三种物质的溶解度由大到小的顺序是A>B>C;(5)A的溶解度受温度的影响较大,当A中含有少量C时,为了得到纯净的A,可采用降温结晶的方法。
所以答案是:(1)30;(2)饱和;(3)不变;(4)A>B>C;(5)降温结晶。
【考点精析】根据题目的已知条件,利用饱和溶液和不饱和溶液和固体溶解度的影响因素的相关知识可以得到问题的答案,需要掌握饱和与不饱和的判断方法:看有无不溶物或继续加入该溶质,看能否溶解;影响固体溶解度的因素:①溶质、溶剂的性质(种类) ②温度:大多数固体物的溶解度随温度升高而升高;如KNO3;少数固体物质的溶解度受温度的影响很小;如NaCl;极少数物质溶解度随温度升高而降低.如Ca(OH)2.

【题目】化肥对提高农作物的产量具有重要的作用,碳铵(碳酸氢铵)就是农民朋友经常使用的一种氮肥,碳铵易溶于水、受潮时常温分解,温度越高分解越快,遇碱时放出氨气。某校化学兴趣小组为测定某碳铵肥料样品的纯度,将8.5g样品加入足量的浓氢氧化钠溶液中共热,(碳铵中的杂质不与氢氧化钠反应,反应的方程式为NH4HCO3+2NaOH = Na2CO3+2H2O+NH3↑),把产生的所有NH3用足量的硫酸溶液吸收,同时测量两分钟内硫酸溶液增加的质量,结果如下表所示。
时间/S | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
增加质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
试回答下列问题:
(1)根据碳酸氢铵的性质,你认为在使用碳铵肥料时应注意的问题是___________________。
(2)请在坐标纸上,以反应时间为横坐标,以产生NH3质量为纵坐标,画出产生气体的质量随时间变化的关系曲线,并判断表中m约为_________________。

(3)试计算该样品中碳酸氢铵的质量分数(写出计算过程,计算结果保留一位小数)。
【题目】常温下,一些食物的近似pH如下:
食物 | 香蕉 | 草莓 | 牛奶 | 鸡蛋清 |
pH | 4.5~4.6 | 3.0~3.5 | 6.3~6.6 | 7.6~8.0 |
下列说法中正确的是
A.香蕉和草莓均显酸性B.牛奶和鸡蛋清均显碱性
C.香蕉比草莓的酸性强D.胃酸过多的人应多食香蕉和草莓