题目内容
某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g.计算:(1)完全反应后生成CO2的质量;
(2)纯碱样品中碳酸钠的质量分数(结果精确到0.1%)
【答案】分析:分析反应可发现,混合物中加入稀盐酸恰好完全反应后,反应前后的质量差即为反应产生二氧化碳的质量;根据反应的化学方程式,由生成二氧化碳的质量计算出混合物质中碳酸钠的质量,碳酸钠质量与样品质量比可计算出纯碱样品中碳酸钠的质量分数.
解答:解:(1)根据质量守恒定律,完全反应后生成二氧化碳的质量=11g+50g-56.6g=4.4g
(2)设参加反应的碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 44
x 4.4g
 x=10.6g
x=10.6g
纯碱样品中碳酸钠的质量分数= ×100%≈96.4%
×100%≈96.4%
答:(1)完全反应后生成CO2的质量为4.4g;(2)纯碱样品中碳酸钠的质量分数约为96.4%.
点评:利用质量守恒定律,计算出反应放出二氧化碳的质量是解决问题的基础.
解答:解:(1)根据质量守恒定律,完全反应后生成二氧化碳的质量=11g+50g-56.6g=4.4g
(2)设参加反应的碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 44
x 4.4g
 x=10.6g
x=10.6g纯碱样品中碳酸钠的质量分数=
 ×100%≈96.4%
×100%≈96.4%答:(1)完全反应后生成CO2的质量为4.4g;(2)纯碱样品中碳酸钠的质量分数约为96.4%.
点评:利用质量守恒定律,计算出反应放出二氧化碳的质量是解决问题的基础.

练习册系列答案
相关题目
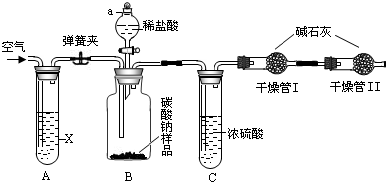
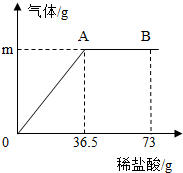 某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答: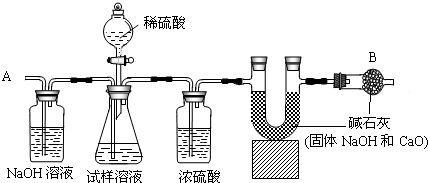
 如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:
如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算: (2013?贵港一模)某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
(2013?贵港一模)某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答: