题目内容
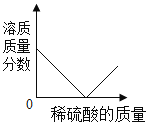
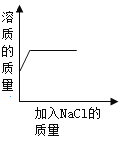
【题目】下图是甲、乙两种物质的溶解度曲线,下列说法正确的是

A.甲、乙两种物质中,乙的溶解度受温度影响比甲的大
B.40℃时甲和乙的饱和溶液,降温至 20℃时仍是饱和溶液
C.40℃时甲和乙各 40g 分别加入 100g 水中,均形成饱和溶液
D.40℃时,将 30g 甲物质加入 50g 水中,充分搅拌后,所得溶液质量为 80g
【答案】B
【解析】
A、甲的溶解度曲线比乙的更陡,所以甲的溶解度受温度变化影响比乙大,故A错误;
B、甲、乙的溶解度均随温度的升高而增大,所以40℃时甲和乙的饱和溶液,降温到20℃时仍为饱和溶液,故B正确;
C、40℃时甲的溶解度是50g,即在40℃时100g水中最多能溶解50g甲,这个时候甲只加了40g,因此并未达到饱和状态,故C错误;
D、40℃时甲的溶解度是50g,即在40℃时100g水中最多能溶解50g甲,所以在此温度下50g水中最多能溶解25g甲,有5g的甲并没有溶解,所以得到的溶液质量为75g,故D错误。
故选B。

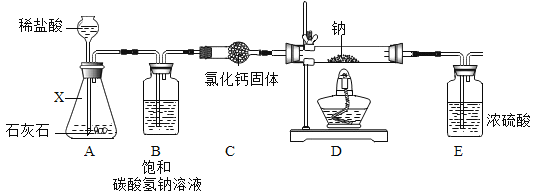
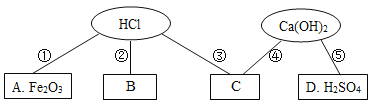
【题目】为探究酸、碱、盐的化学性质,某兴趣小组做了如下实验。

试回答下列问题
(1)试管A中的现象是______________________。
(2)试管B中反应的化学方程式为_____________________________。
(3)甲同学把反应后的C、D试管中的废液倒入一只洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成;过滤后得到白色沉淀和无色滤液。甲同学欲探究无色滤液中溶质的成分。
(提出问题)无色滤液中的溶质是什么?
(作出猜想)
猜想I NaCl
猜想I I NaCl和CaCl2
猜想Ⅲ NaCl 和Na2CO3
猜想IV:NaCl 、CaCl2 和Na2CO3
小明认为猜想IV定不成立,其原因是____________________(用化学方程式表示)。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
i.取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想____成立 |
ⅱ.取少量滤液于试管中,滴加少量____ | 有气泡产生 |