题目内容
学校实验室内有瓶放置时间较长的过氧化氢溶液,为测算该溶液中过氧化氢的质量分数:现取50g样品,加入2g MnO2完全反应后,剩余物质质量为50.4g。
计算(1)生成氧气的质量。
(2)样品中过氧化氢的质量分数。
(1)1.6g(1分)(2)6.8%
解析试题分析:(1)根据质量守恒定律反应前后质量不变可知,生成的氧气的质量为:50g+2g-50.4g=1.6g
(2)解:设过氧化氢的质量为x
2 H2O2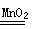 2H2O+ O2 ↑
2H2O+ O2 ↑
68 32
X 1.6g
68:32=x:1.6g
解得 x="3.4g"
3.4g ÷ 50g × 100% =" 6.8%"
答:生成氧气的质量为1.6g;样品中过氧化氢的质量分数为6.8%
考点:根据化学方程式的计算

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
请回答下列问题。
(1)为减少龋齿,制造口香糖时常用木糖醇(C5H12O5)代替蔗糖。
①木糖醇的相对分子质量 ,木糖醇中碳元素的质量分数 。
②一个木糖醇分子中有 个原子,分子中碳、氢、氧原子的个数比为 。
(2)① 克丙烯酰胺(C3H5ON)与9克尿素CO(NH2)2所含的氮元素质量相等。
②根据表中数据计算,每500克该加碘食盐中碘酸钾KIO3的质量范围是
| 配料表:氯化钠、碘酸钾 净含量:500克 碘含量(以I计):30~60mg/kg |
A、15~30mg B、25~51mg C、60~120mg
③碘元素对青少年智力发育影响很大,如图超市销售的一种加碘盐标签上的部分文字说明。中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg。假设碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为 克。

将18g高锰酸钾加热,当产生1.6g氧气时,固体剩余物是 ( )
| A.KMnO4 MnO2 | B.K2MnO4 MnO2 |
| C.KMnO4 MnO2 K2MnO4 | D.KMnO4 K2MnO4 |
质量相同的下列金属,分别加入到足量的稀硫酸中充分反应,放出氢气最多的是 ( )
| A.Na | B.Al | C.Cu | D.Zn |
将ag铁和碳的混合物在氧气中充分灼烧,冷却,称量,发现剩余固体的质量仍为ag,该混合物中碳的质量分数为( )
| A.30.0% | B.22.2% | C.27.6% | D.10.3% |