题目内容
除去下列物质中的少量杂质,所选试剂及操作都正确的是……………………( )
| 选项 | 物质 | 杂质(少量) | 试 剂 | 操作方法 |
| A | Cu | CuO | O2 | 加热 |
| B | 氯化钙溶液 | 盐酸 | 过量的碳酸钙 | 过滤 |
| C | 氯化钠 | 纯碱 | 适量的稀盐酸 | 溶解、过滤、蒸发 |
| D | H2O | 悬浮物 | 明矾 | 吸附 |
B
试题分析:物质的除杂有2个原则:1、加入的物质或采取的方法只能除去杂质,2、在除杂过程中不能引入新的杂质,方法既可以物理手段也可以采用化学方法,A、除去Cu中的CuO,通入氧气,铜会与氧气反应,而要除去的是CuO,故错误,B、除去氯化钙溶液中的盐酸,加入过量的碳酸钙,发生反应:CaCO3+2HCl==CaCl2+H2O+CO2↑,再过滤,即可得到氯化钙溶液,错误,C、除去NaCl中Na2CO3,加入硝酸,发生反应:Na2CO3+2HNO3==2NaNO3+H2O+CO2↑,可除去,但没有必要进行过滤操作,因为没有不溶性的物质,错误,D、除去H2O中悬浮物,加入明矾,利用明矾溶于水形成胶状物吸附水中的杂质,再过滤,即可除去,没有过滤操作,故选B

练习册系列答案
相关题目
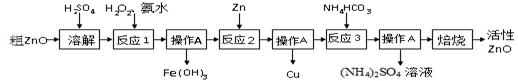
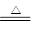 ZnO+CO2↑ Zn(OH)2
ZnO+CO2↑ Zn(OH)2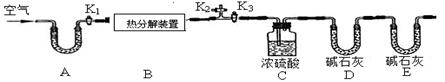
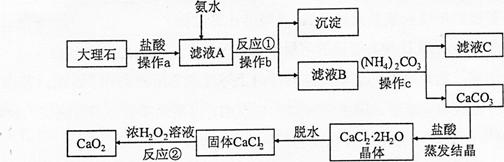
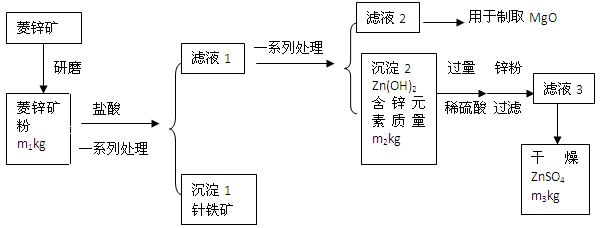
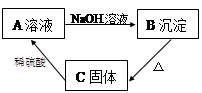
 B_____________________。
B_____________________。