题目内容
下列对实验结果的分析中,错误的是( )
| A、配制食盐溶液时,如果量取水时俯视读数,则所取水的体积偏小 |
| B、点燃氢气时发生爆炸,可能是因为没有检验氢气的纯度 |
| C、将带火星的木条伸入集气瓶内,木条复燃,证明瓶内已集满氧气 |
| D、在测定空气中氧气的体积分数时,充分反应后,需将装置冷却至室温再读数,否则测量结果偏低 |
考点:一定溶质质量分数的溶液的配制,空气组成的测定,氧气的检验和验满,氢气、一氧化碳、甲烷等可燃气体的验纯
专题:常见仪器及化学实验基本操作
分析:A、根据量筒使用的方法分析:俯视读数偏大,量取的水比实际需要的水少;
B、利用不纯的氢气在爆炸极限内遇火会发生爆炸分析;
C、利用检验气体是否收集满要将带火星的木条放在集气瓶口检验不能伸入瓶内分析;
D、利用测定空气中氧气的体积分数的注意事项分析.
B、利用不纯的氢气在爆炸极限内遇火会发生爆炸分析;
C、利用检验气体是否收集满要将带火星的木条放在集气瓶口检验不能伸入瓶内分析;
D、利用测定空气中氧气的体积分数的注意事项分析.
解答:解:A、俯视读数偏大,因此量取的水比实际需要的水少,故A说法正确;
B、不纯的氢气在爆炸极限内遇火会发生爆炸,因此使用前要检验氢气的纯度,故B说法正确;
C、检验气体是否收集满要将带火星的木条放在集气瓶口检验不能伸入瓶内,故C说法不正确;
D、测定空气中氧气的体积分数要等装置冷却才能准确测出氧气的体积分数,否则测量结果偏低,故D说法正确.
故选:C.
B、不纯的氢气在爆炸极限内遇火会发生爆炸,因此使用前要检验氢气的纯度,故B说法正确;
C、检验气体是否收集满要将带火星的木条放在集气瓶口检验不能伸入瓶内,故C说法不正确;
D、测定空气中氧气的体积分数要等装置冷却才能准确测出氧气的体积分数,否则测量结果偏低,故D说法正确.
故选:C.
点评:本题属于基础性的考查,明确量筒的使用方法、气体验满和检验的区别、测定氧气的注意事项等是解题的关键,实验操作的规范性是实验成功的关键,要规范操作才能事半功倍.

练习册系列答案
相关题目
下列实验操作正确的是( )
A、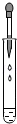 滴加液体 |
B、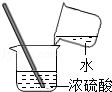 稀释浓硫酸 |
C、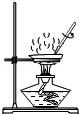 蒸发 |
D、 熄灭酒精灯 |
日常生活中的下列变化,属于物理变化的是( )
| A、工业上分离液态空气制氧气 |
| B、用蜡烛制取炭黑 |
| C、工业上用纯碱制取烧碱 |
| D、用氢氧化钠溶液浸泡,制作叶脉书签 |
某水溶液中含有以下离子中的若干种:K+、Cl-、Ca2+、Zn2+、CO32-、SO42-,现取两份溶液各100mL分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有沉淀产生.根据上述实验,以下有关原溶液的论断不正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有沉淀产生.根据上述实验,以下有关原溶液的论断不正确的是( )
| A、Cl-一定存在 |
| B、CO32-和SO42-一定存在,且二者的个数比为1:2 |
| C、Zn2+ 和Ca2+一定不存在 |
| D、100mL溶液中K+的质量不小于2.34g |
许多物质在溶液中都以离子形式存在.我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀的一类化学反应.如:氢氧化钠与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程.结合信息,你认为下列各组离子间不能反应的是( )
| A、H+Na+ OH- N03- |
| B、Na+ K+ Cl- OH- |
| C、H+ K+ CO32-HCO3- |
| D、K+Ba2+Cl-SO42- |
下列变化属于物理变化的是( )
| A、活性碳使红墨水褪色 |
| B、浓硫酸使纸变黑 |
| C、工业上常用稀硫酸除铁锈 |
| D、盐酸能使紫色石蕊溶液变红 |
下列物质长时间放置在空气中,质量会增加且变质的是( )
| A、浓盐酸 | B、浓硫酸 |
| C、氧化钙 | D、食盐 |
实验室用98%的浓硫酸(密度1.84g/cm3)配制一定溶质质量分数的稀硫酸,不需要的仪器是( )
| A、玻璃棒 | B、量筒 |
| C、烧杯 | D、托盘天平 |