题目内容
【题目】现有如图所示实验装置,请回答下列问题
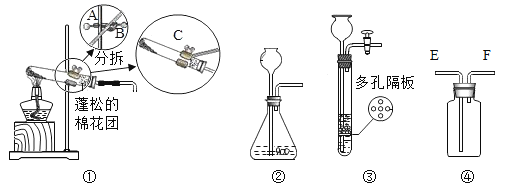
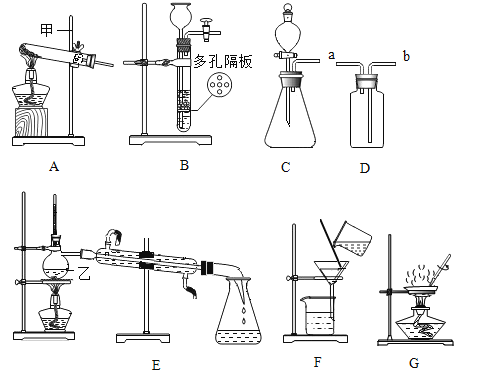
(1)实验室用高锰酸钾制取氧气,通常选用的A装置作为发生装置,反应的化学方程式是_____,在固定试管时,若发现试管口没有略向下倾斜,应调整铁夹_____部位(填A或B或C)。若用装置④收集氧气,气体应该从_____端导入。
(2)用块状固体和液体常温下制取气体时,用装置③代替装置②的优点是_____。
(3)观察装置③的反应,判断气体制取处于_____(填“进行”或“停止”)中。
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ B E 可以控制反应的发生与停止 进行
K2MnO4+MnO2+O2↑ B E 可以控制反应的发生与停止 进行
【解析】
(1)根据反应物的状态和反应条件选择发生装置:固体加热型和固液常温型;加热高锰酸钾制取氧气,产生锰酸钾、二氧化锰和氧气,写出反应的方程式;根据铁架台固定铁夹的方法分析;根据氧气的密度比空气大确定进气口;
(2)根据装置图③分析,可以控制反应的发生与停止;
(3)根据装置中隔板的作用分析优点及固液接触情况分析反应的情况。
(1)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气;在固定试管时,若发现试管口没有略向下倾斜,应调整铁夹B部位;氧气的密度比空气大,用用装置④收集时,氧气从长管进入;故填:2KMnO4![]() K2MnO4+MnO2+O2↑;B;E;
K2MnO4+MnO2+O2↑;B;E;
(2)装置③代替装置②多了一个隔板可以放置固体,利用气压通过活塞的开关可以控制固液的接触和分离,从而控制反应的发生和停止,所以优点是:随时控制反应发生或停止(随开随关);故填:可以控制反应的发生与停止;
(3)由于该装置中的液面高于固体,所以反应正在进行。故填:进行。

【题目】下列实验设计能达到实验目的是( )
选项 | A | B | C | D |
实 验 设 计 |
|
|
|
|
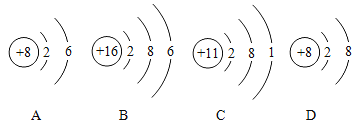
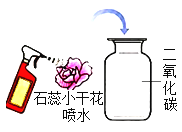
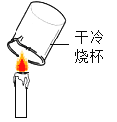
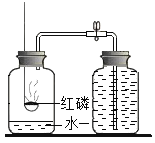
实验 目的 | 探究CO2与H2O是否发生反应 | 探究石蜡中含有氢元素和碳元素 | 测定空气中氧气的含量 | 证明铁生锈是水和氧气共同作用的结果 |
A. AB. BC. CD. D
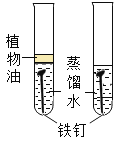
【题目】某兴趣小组发现铁钉生锈需要几天的时间,询问老师如何加快铁钉生锈的速度。
老师说氯化物可能加快铁钉生锈的速度。
【提出问题】氯化物对铁钉生锈有怎样的影响?
【查阅资料】
ⅰ.NaCl、CaCl2、CuCl2等由氯离子与金属离子构成的盐属于氯化物。
ⅱ.铜能与氧气反应,生成黑色的CuO。
ⅲ.CuO能与稀硫酸发生反应:CuO + H2SO4 ==== CuSO4 + H2O。
【进行实验、分析解释、获得结论】
实验1:探究氯化物对铁钉生锈速度的影响。
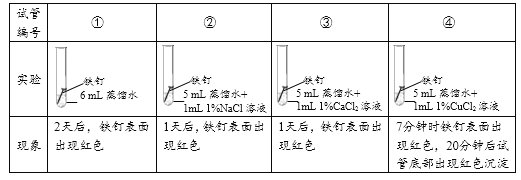
(1)对比实验①②③可以得到的结论是_________。
(2)小组同学认为,试管④中的红色沉淀可能是铁锈,也可能是铜。他们认为红色沉淀可能是铜的理由是__________(用化学方程式解释)。
实验2:探究试管④中红色沉淀的物质组成。
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 取出试管④中的铁钉,过滤剩余物,洗涤滤纸上的物质 | 固体为红色 |
Ⅱ | 将步骤Ⅰ所得红色固体加入试管中,再向试管中加入足量的___________ | 红色固体大部分溶解,溶液变为黄色 |
Ⅲ | 将步骤Ⅱ所得混合物过滤,洗涤、干燥滤纸上的固体后,置于石棉网上充分加热 | 红色固体变黑 |
Ⅳ | 向试管中加入步骤Ⅲ所得黑色固体,再加入足量稀硫酸 | 黑色固体全部溶解,溶液变为蓝色 |
(3)步骤Ⅱ中所加入的试剂是_________。
(4)步骤Ⅲ、Ⅳ的实验目的是_________。
(5)由实验2可得出结论:试管④中红色沉淀的物质组成是_________。
【反思与评价】
(6)结合实验1、2的结论,对于“氯化物对铁钉生锈速度的影响”,小组同学提出了进一步的假设:__。