题目内容
【题目】现有一家庭食用纯碱样品,其中含杂质氯化钠(不含其它杂质),为了测定样品中杂质氯化钠的质量分数,李明同学进行了三次实验。实验如下表:
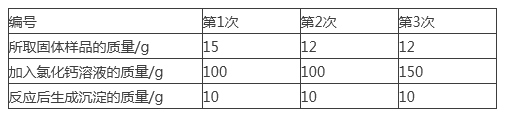
完成下列计算(计算结果精确到0.1%):
(1)样品中氯化钠的质量分数;
(2)加入氯化钙溶液的溶质质量分数;
(3)恰好完全反应时,反应后所得溶液中氯化钠的质量分数。
【答案】(1)11.7%;(2)11.1%;(3)12.8%
【解析】由3次实验比较可知,第2次实验氯化钙和碳酸钠恰好完全反应,设12g固体样品中碳酸钠的质量为x ,100g氯化钙溶液中溶质的质量为y,生成氯化钠的质量为m
Na2CO3+CaCl2=2NaCl+CaCO3![]()
106 111 117 100
X y m 10g
![]() =
=![]() =
=![]() =
=![]()
得:x=10.6g,y=11.1g,m=11.7g,
故样品中氯化钠的质量分数为: ![]() =11.7%
=11.7%
氯化钙溶液中的溶质的质量分数为:11.1g![]() 11.1%
11.1%
恰好完全反应时,反应后所得溶液中氯化钠的质量分数(11.7g+12g-10.6g)![]() (100g+12g-10g)
(100g+12g-10g)![]() =12.8%
=12.8%
答:样品中氯化钠的质量分数为11.7%,氯化钙溶液中的溶质的质量分数为11.7%,恰好完全反应时,反应后所得溶液中氯化钠的质量分数为12.8%。

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目