题目内容
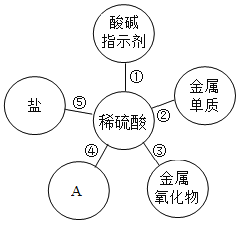
【题目】A、B、C、D、E、F、G是初中化学中常见的物质,其中A、D、G是单质,其他是化合物。C是天然气的主要成分,F的水溶液呈蓝色,G是目前产量最大的金属,图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去)。
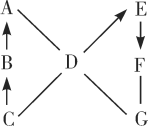
(1)物质C的化学式为_____。
(2)图中涉及复分解反应的化学方程式可能是_____;四种基本反应类型中,图中涉及_____种。
(3)G在D中反应时的现象是_____。
(4)某工厂欲从只含有硫酸铜的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
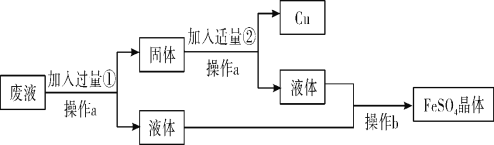
①操作a、b的名称分别是_____、_____。
②写出流程中有关反应的其中一个化学方程式:_____。该反应能够发生的原因是_____。
【答案】CH4 CuO+H2SO4=CuSO4+H2O 4 剧烈燃烧,火星四射,有黑色固体生成,放出热量 过滤 蒸发 Fe+CuSO4=FeSO4+Cu(或Fe+H2SO4=FeSO4+H2↑) 在金属活动性顺序中,铁位于铜(氢)之前
【解析】
C是天然气的主要成分,化学式是CH4;甲烷可以制取B,甲烷燃烧生成二氧化碳和水,B又能制取A单质,所以B是水,A是氢气。F的水溶液呈蓝色,可以是硫酸铜溶液,G是目前产量最大的金属,则G是铁,E能制取硫酸铜,说明E是铜的化合物,可以是氧化铜,代入验证符合题意。
(1)由分析可知C为甲烷,故填:CH4。
(2)由分析可知E为氧化铜,F为硫酸铜,图中涉及复分解反应的化学方程式可能是CuO+H2SO4=CuSO4+H2O,由分析可知B为水,A为氢气,B 生成A水通电分解氢气氧气,属于分解反应,D为氧气,A和D反应属于化合反应,F是硫酸铜,G为铁,属于置换反应,故涉及4中反应类型,故填:CuO+H2SO4=CuSO4+H2O;4。
(3)由分析可知G是铁D为氧气G在D中反应时的现象是剧烈燃烧,火星四射,有黑色固体生成,放出热量,故填:剧烈燃烧,火星四射,有黑色固体生成,放出热量。
(4)①经过操作a能得到固体和液体,故a操作为过滤,从液体中得到晶体可以是蒸发操作,故填:过滤;蒸发。
②经过过滤操作得到的液体中能得到硫酸亚铁,说明回收铜时加入的是铁,多余的铁与硫酸反应生成硫酸亚铁,该反应能够发生的原因是在金属活动性顺序中,铁位于铜(氢)之前,故填:Fe+CuSO4=FeSO4+Cu或Fe+H2SO4=FeSO4+H2↑;在金属活动性顺序中,铁位于铜(氢)之前。