题目内容
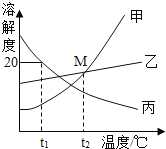
【题目】下列曲线示意图不正确的是()
A.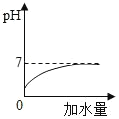 向稀盐酸中加蒸馏水(图中 q 曲线未与虚线相交,只无限接近)
向稀盐酸中加蒸馏水(图中 q 曲线未与虚线相交,只无限接近)
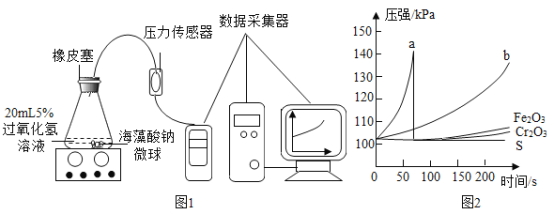
B. 等体积、等质量分数的过氧化氢分解
等体积、等质量分数的过氧化氢分解
C.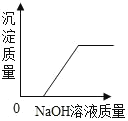 HCl 和 FeCl3的混合液中加入 NaOH 溶液
HCl 和 FeCl3的混合液中加入 NaOH 溶液
D.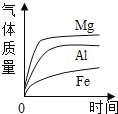 等质量、等颗粒大小的金属加入足量稀盐酸
等质量、等颗粒大小的金属加入足量稀盐酸
【答案】D
【解析】
A、酸溶液的 pH 小于 7,加水稀释酸性减弱,其 pH 会增大,但是不会大于或等于 7,故 A 正确;
B、过氧化氢溶液中加入二氧化锰能加快反应速度,但生成氧气的质量相同,故 B 正确;
C、盐酸与氯化铁的混合物中加入氢氧化钠,盐酸和氢氧化钠反应生成氯化钠和水,氯化铁与氢氧化钠反应生成氢氧化铁沉淀,生成的氢氧化铁能与盐酸反应生成氯化铁,故在 盐酸与氯化铁的混合物中加入氢氧化钠,得等一段时间才能生成氢氧化铁沉淀,故 C 正确;
D、等质量的镁、铝、铁与足量盐酸反应生成的氢气质量铝最多,不是镁,故 D 错误。
故选:D。

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】如图是某食品包装中的干燥剂。

下面是兴趣小组对干燥剂的探究过程,请参与到其中去,回答下列有关问题:
(1)干燥剂能吸水的原因是_____(用化学方程式表示)。
(2)同学们对放置一段时间干燥剂的成分进行探究
(提出问题)干燥剂现在的成分是什么?
(猜想)猜想1:含有CaO 猜想2:含有Ca(OH)2 猜想3:含有CaCO3
(进行实验)
实验步骤 | 实验现象 | 结论 |
1.取少量干燥剂于试管中,向试管中加入少量的水,用手触摸试管外壁 | 试管外壁有热感 | 含有_____ |
2.向步骤1加水后的试管中滴入无色酚酞试液 | 无色酚酞试液变红色 | 含有Ca(OH)2 |
3.向步骤2反应后的试管中加入足量的______ | _____ | 含有CaCO3,反应的化学方程式是______ |
(实验分析)小明同学认为步骤2不能确定Ca(OH)2是否存在,原因是_____。
(改进实验)小明同学进行下列实验

根据小明的实验结果,干燥剂中含有的物质是_____。
【题目】K2CO3和KNO3在不同温度时的溶解度如下。
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度(g/100g 水) | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
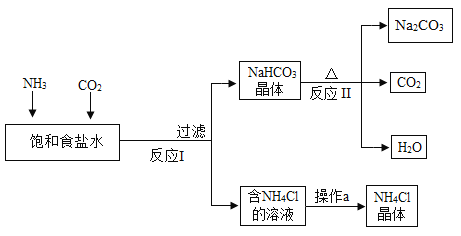
某KNO3样品中含有少量K2CO3,其提纯过程如下:
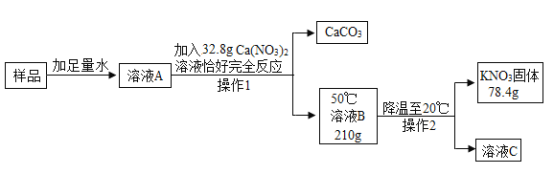
①提纯过程中涉及的化学反应方程式是_____。
②溶液 A 中加 Ca(NO3)2溶液恰好完全反应的目的是_____。下列试剂中可以替代Ca(NO3)2 溶液的是_____(填字母)。
a CaCl2 b Ba(NO3)2 c Ca(OH)2 d BaCl2
③溶液A、B、C 中,一定属于饱和溶液的是_____(填字母)。
④样品中钾元素的质量为_____g(精确到0.1)。
⑤若要测定样品中KNO3 的纯度,还需测定的量是_____。
【题目】闽东毗邻东海,海洋资源十分丰富.从海水中提取氯化钠并以氯化钠和水为原料制取氢氧化钠、氯气等物质的工艺流程图如下:
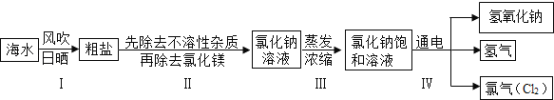
某兴趣小组进行如下实验:
(实验一)除去粗盐中的不溶性杂质
步骤一:用托盘天平称取5.0g粗盐,用药匙将该粗盐逐渐加入盛10mL水的烧杯中,边加边用玻璃棒搅拌,一直加到粗盐不再溶解为止.称量剩下的粗盐质量为1.4g
步骤二:经过过滤、蒸发,得到3.2g精盐.
(1)计算精盐的产率_________(保留一位小数).
(2)该小组测得的产率偏低,可能的原因是________.
A溶解时未充分搅拌
B蒸发时水分未蒸干
C蒸发时盐粒溅出蒸发皿
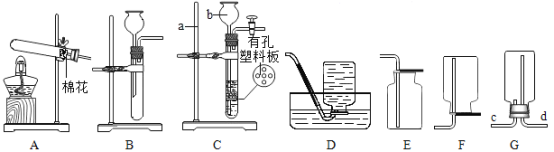
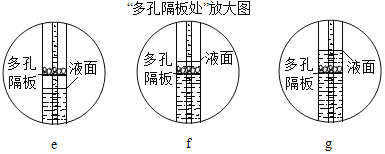
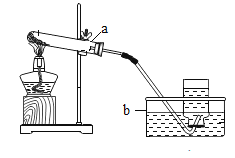
(3)步骤一、二的部分操作如图所示,其中错误的是_________(填字母序号).
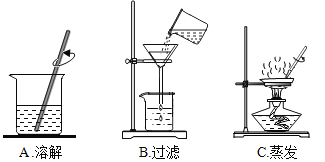
(实验二)探究工艺流程图步骤Ⅱ所得的氯化钠溶液中MgCl2是否除尽,溶液中是否含有CaCl2
[查阅资料]有关物质的溶解性表(20℃)
阴离子 | OH﹣ |
|
Ca2+ | 微 | 不 |
Mg2+ | 不 | 微 |
[进行实验]请你与他们共同完成,并回答所给的问题:
实验步骤 | 实验现象 | 实验结论 |
步骤一:取一定量的氯化钠溶液于试管中,加入适量的NaOH溶液 | 无明显现象 | 说明MgCl2______(填“已”或“未”)除尽 |
步骤二:往步骤一所得溶液中加入适量的______溶液 | 产生白色沉淀 | 说明溶液中含有CaCl2 |
[拓展思维]
(1)工艺流程图步骤Ⅰ从海水中得到粗盐,采用风吹日晒蒸发溶剂的方法,而不是采用降低溶液温度的方法,原因是________________________________.
(2)写出工艺流程图步骤Ⅳ的化学方程式__________________________.