题目内容
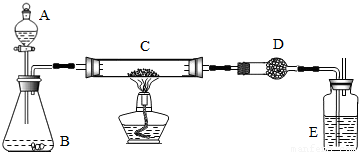
某课外活动小组用加热碳粉(过量)和氧化铜的混合物的方法制得铜粉样品后,再用下图装置对得的样品进行实验.图中铁加台等装置已略去.请帮助他们完成下列实验报告.
(一)实验目的:______
(二)实验用品:
仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品,过氧化氢溶液、二氧化锰、碱石灰、浓硫酸
(三)实验内容
| 实验过程 | 实验现象 | 有关化学方程式 |
| 在C中加入样品Wg,D中装入药品后称量为m1g.连接好仪器后,检查装置气密性. | ||
| 打开A的活塞,慢慢滴加溶液 | ||
| 对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热 | ||
| 冷却后,称量D的质量为m2g |
(五)问题和讨论:
实验完成后,教师评议说:按上述实验设计,即使C中反应完全、D中吸收完全、所得的结果也会有误差.经过讨论,有同学提出在B与C之间增加一个装置.再次实验后,得到了较为正确的结果. 原实验所结果不够准确的原因可能是______,在B与C之间增加的装置和其中盛放的药品可以是______.
【答案】分析:(一)根据实验过程和实验装置来判断实验目的;
(三)根据铜和碳的化学性质及各装置的用途来判断每一步骤中现象并写出化学方程式;
(四)根据图中装置及实验目的可以知道D装置是用来吸收二氧化碳的,所以可以根据碳元素的质量守恒来完成该题的解答;
(五)吸收二氧化碳用碱石灰,而反应开始生成的气体会带出一部分水蒸气,从而使反应后称量的D装置的质量增加,可以据此完成该题的解答.
解答:解:(一)实验中用的是过量的碳粉来还原氧化铜的,所以制得的铜中含有碳粉,那么该实验的目的就是来探究铜粉在混合物中的质量分数的;
(三)根据实验目的可以知道若验证铜的质量分数,可以用氧气来与之反应,然后测量质量进行求算,所可以判断在B中所发生的反应为过氧化氢溶液和二氧化锰的反应,所以可以知道该装置中所发生的反应为过氧化氢和二氧化锰的反应,故可以写出化学方程式,而实验现象为:在B和E装置中产生气泡,生成的氧气通入被加热的碳粉和铜粉的混合物中,铜和碳都会和氧气反应,以可以写出该反应的化学方程式,所以原来红色的铜和黑色的碳组成的混合物要全部变为黑色;
(四)根据(三)可以知道D管吸收了二氧化碳,所以可以知道D管的质量变化即为生成的气体二氧化碳的质量,根据质量守和定律可以知道,二氧化碳中的碳的质量即为碳粉的质量,所以碳的质量=(m2-m1)×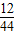 ×100%,那么铜的质量分数为:
×100%,那么铜的质量分数为: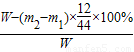 ×100%;
×100%;
(五)过氧化氢溶液分解产生的氧气逸出时会带出一部分水蒸气,被D装置吸收,而使测得的二氧化碳气体的质量增加,即碳的质量增加,所以会使测量结果偏小,为了防止水蒸气影响实验结果,可以在B和C之间加一个盛有浓硫酸的洗气瓶来吸收水蒸气,从而使结果尽可能的准确.
故答案为:(一)测定铜粉在混合物中的质量分数;
(三)
(四)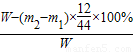 ×100%;
×100%;
(五)双氧水分解后产生的氧气会带出一部分水蒸气,通过C后被D吸收,而使m2的值增大,而使测得的铜的质量分数偏小;盛有浓硫酸的洗气瓶.
点评:熟练掌握碳和铜的化学性质,知道氧气的实验室制法并会书写化学方程式,对于用固体和液体制取气体的方法,在生成气体时容易带出水蒸气,如果水蒸气能够干扰实验现象要注意对气体进行干燥,防止干扰实验现象.
(三)根据铜和碳的化学性质及各装置的用途来判断每一步骤中现象并写出化学方程式;
(四)根据图中装置及实验目的可以知道D装置是用来吸收二氧化碳的,所以可以根据碳元素的质量守恒来完成该题的解答;
(五)吸收二氧化碳用碱石灰,而反应开始生成的气体会带出一部分水蒸气,从而使反应后称量的D装置的质量增加,可以据此完成该题的解答.
解答:解:(一)实验中用的是过量的碳粉来还原氧化铜的,所以制得的铜中含有碳粉,那么该实验的目的就是来探究铜粉在混合物中的质量分数的;
(三)根据实验目的可以知道若验证铜的质量分数,可以用氧气来与之反应,然后测量质量进行求算,所可以判断在B中所发生的反应为过氧化氢溶液和二氧化锰的反应,所以可以知道该装置中所发生的反应为过氧化氢和二氧化锰的反应,故可以写出化学方程式,而实验现象为:在B和E装置中产生气泡,生成的氧气通入被加热的碳粉和铜粉的混合物中,铜和碳都会和氧气反应,以可以写出该反应的化学方程式,所以原来红色的铜和黑色的碳组成的混合物要全部变为黑色;
(四)根据(三)可以知道D管吸收了二氧化碳,所以可以知道D管的质量变化即为生成的气体二氧化碳的质量,根据质量守和定律可以知道,二氧化碳中的碳的质量即为碳粉的质量,所以碳的质量=(m2-m1)×
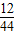 ×100%,那么铜的质量分数为:
×100%,那么铜的质量分数为: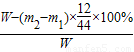 ×100%;
×100%;(五)过氧化氢溶液分解产生的氧气逸出时会带出一部分水蒸气,被D装置吸收,而使测得的二氧化碳气体的质量增加,即碳的质量增加,所以会使测量结果偏小,为了防止水蒸气影响实验结果,可以在B和C之间加一个盛有浓硫酸的洗气瓶来吸收水蒸气,从而使结果尽可能的准确.
故答案为:(一)测定铜粉在混合物中的质量分数;
(三)
| 实验过程 | 实验现象 | 有关化学方程式 |
| 在C中加入样品Wg,D中装入药品后称量为m1g.连接好仪器后,检查装置气密性. | ||
| 打开A的活塞,慢慢滴加溶液 | 装置B和E中有气泡冒出 | 2H2O2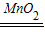 2H2O+O2↑ 2H2O+O2↑ |
| 对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热 | 灰黑色的固体逐渐变为黑色 | C+O2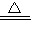 CO2 CO22Cu+O2 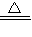 2CuO 2CuO |
| 冷却后,称量D的质量为m2g |
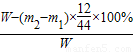 ×100%;
×100%;(五)双氧水分解后产生的氧气会带出一部分水蒸气,通过C后被D吸收,而使m2的值增大,而使测得的铜的质量分数偏小;盛有浓硫酸的洗气瓶.
点评:熟练掌握碳和铜的化学性质,知道氧气的实验室制法并会书写化学方程式,对于用固体和液体制取气体的方法,在生成气体时容易带出水蒸气,如果水蒸气能够干扰实验现象要注意对气体进行干燥,防止干扰实验现象.

练习册系列答案
相关题目
某课外活动小组用加热碳粉(过量)和氧化铜的混合物的方法制得铜粉样品后,再用下图装置对得的样品进行实验.图中铁加台等装置已略去.
请帮助他们完成下列实验报告.
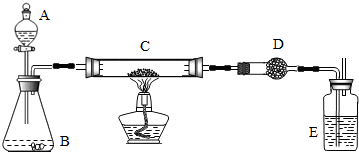
(一)实验目的:
(二)实验用品:
仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品,过氧化氢溶液、二氧化锰、碱石灰、浓硫酸
(三)实验内容
(四)计算:样品中铜的质量分数= (用含W,m1\m2的代数式表示).
(五)问题和讨论:
实验完成后,教师评议说:按上述实验设计,即使C中反应完全、D中吸收完全、所得的结果也会有误差.经过讨论,有同学提出在B与C之间增加一个装置.再次实验后,得到了较为正确的结果. 原实验所结果不够准确的原因可能是 ,在B与C之间增加的装置和其中盛放的药品可以是 .
请帮助他们完成下列实验报告.

(一)实验目的:
(二)实验用品:
仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品,过氧化氢溶液、二氧化锰、碱石灰、浓硫酸
(三)实验内容
| 实验过程 | 实验现象 | 有关化学方程式 |
| 在C中加入样品Wg,D中装入药品后称量为m1g.连接好仪器后,检查装置气密性. | ||
| 打开A的活塞,慢慢滴加溶液 | ||
| 对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热 | ||
| 冷却后,称量D的质量为m2g |
(五)问题和讨论:
实验完成后,教师评议说:按上述实验设计,即使C中反应完全、D中吸收完全、所得的结果也会有误差.经过讨论,有同学提出在B与C之间增加一个装置.再次实验后,得到了较为正确的结果. 原实验所结果不够准确的原因可能是
某课外活动小组用加热碳粉(过量)和氧化铜的混合物的方法制得铜粉样品后,再用下图装置对得的样品进行实验.图中铁加台等装置已略去.
请帮助他们完成下列实验报告.
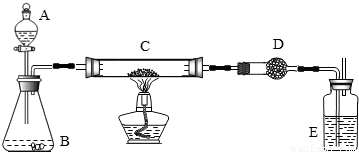
(一)实验目的:______
(二)实验用品:
仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品,过氧化氢溶液、二氧化锰、碱石灰、浓硫酸
(三)实验内容
(四)计算:样品中铜的质量分数=______(用含W,m1\m2的代数式表示).
(五)问题和讨论:
实验完成后,教师评议说:按上述实验设计,即使C中反应完全、D中吸收完全、所得的结果也会有误差.经过讨论,有同学提出在B与C之间增加一个装置.再次实验后,得到了较为正确的结果. 原实验所结果不够准确的原因可能是______,在B与C之间增加的装置和其中盛放的药品可以是______.
请帮助他们完成下列实验报告.

(一)实验目的:______
(二)实验用品:
仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品,过氧化氢溶液、二氧化锰、碱石灰、浓硫酸
(三)实验内容
| 实验过程 | 实验现象 | 有关化学方程式 |
| 在C中加入样品Wg,D中装入药品后称量为m1g.连接好仪器后,检查装置气密性. | ||
| 打开A的活塞,慢慢滴加溶液 | ||
| 对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热 | ||
| 冷却后,称量D的质量为m2g |
(五)问题和讨论:
实验完成后,教师评议说:按上述实验设计,即使C中反应完全、D中吸收完全、所得的结果也会有误差.经过讨论,有同学提出在B与C之间增加一个装置.再次实验后,得到了较为正确的结果. 原实验所结果不够准确的原因可能是______,在B与C之间增加的装置和其中盛放的药品可以是______.
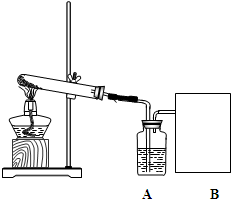 (2006?菏泽)某课外活动小组用氯酸钾和二氧化锰的混合物制取干燥、较纯净的氧气.实验步骤如下:
(2006?菏泽)某课外活动小组用氯酸钾和二氧化锰的混合物制取干燥、较纯净的氧气.实验步骤如下: