题目内容
【题目】根据下列反应事实写出相应的化学方程式。
(1)铝在空气中表面易生成一层致密的氧化膜_____;
(2)氢氧化钠溶液和硫酸铜溶液混合_____;
(3)铝壶不易用稀盐酸长时间浸泡_____;
(4)一种固体加热分解后没有固体残留的反应_____;
(5)久置石灰水的表面出现一层白膜_____。
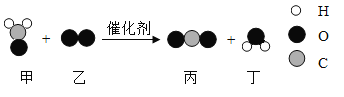
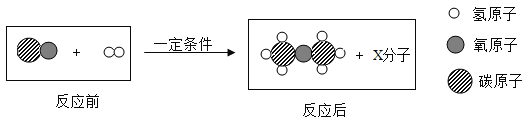
(6)利用乙炔(C2H2) 完全燃烧放热多,氧炔焰用于金属切割和焊接_____。
【答案】4Al+3O2=2Al2O3 2NaOH+CuSO4=Na2SO4+Cu(OH)2↓ 2Al+6HCl=2AlCl3=3H2↑ NH4HCO3![]() NH3↑+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O 2C2H2+5O2
NH3↑+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O 2C2H2+5O2![]() 4CO2+2H2O
4CO2+2H2O
【解析】
(1)铝在空气中表面易生成一层致密的氧化铝薄膜:4Al+3O2=2Al2O3;
(2)氢氧化钠溶液和硫酸铜溶液混合生成硫酸钠溶液和氢氧化铜沉淀:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;
(3)铝壶不易用稀盐酸长时间浸泡反应生成氯化铝和氢气:2Al+6HCl=2AlCl3=3H2↑;
(4)碳酸氢铵固体加热分解后没有固体残留的反应:NH4HCO3![]() NH3↑+H2O+CO2↑;
NH3↑+H2O+CO2↑;
(5)久置石灰水与空气中的二氧化碳梵音个,表面出现一层白膜:CO2+Ca(OH)2=CaCO3↓+H2O;
(6)利用乙炔(C2H2) 完全燃烧放热多,氧炔焰用于金属切割和焊接:2C2H2+5O2![]() 4CO2+2H2O。
4CO2+2H2O。

 53随堂测系列答案
53随堂测系列答案【题目】小明同学为了在实验室制备二氧化碳并探究二氧化碳的性质,进行了以下实验探究。
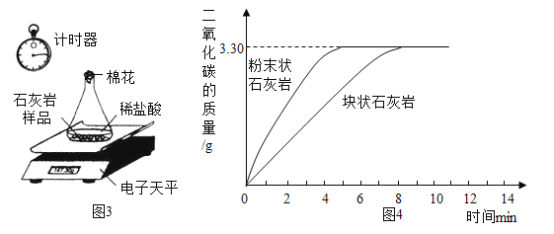
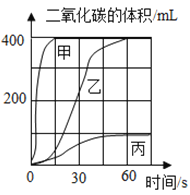
[实验一]选用药品。按下表进行实验.取等质量的大理石加入足量酸中(杂质不与酸反应).产生二氧化碳体积随时间变化曲线如图所示:
实验编号 | 药品 |
Ⅰ | 块状大理石、10%硫酸 |
Ⅱ | 块状大理石、7%盐酸 |
Ⅲ | 大理石粉末、7%盐酸 |
(1)图中丙对应实验______ (选 填“Ⅰ”“Ⅱ”或“Ⅲ”)。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是___________________。不用甲对应的药品,理由是_____________。
[实验二]性质探究。如图所示。用软塑料瓶进行实验
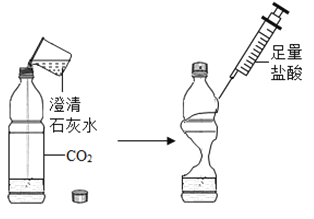
(2)向瓶中倒入澄清石灰水,观察到软塑料瓶变瘪,澄清石灰水变浑浊。反应的化学方程式为__________________。
(3)再向瓶中注人足量盐酸,观察到的现象有。浑浊消失,__________________。
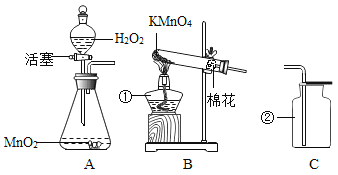
[实验拓展]如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为用石蕊溶液染成紫色的干燥棉球。开始通气时④变红,通气一段时间后①变红.②③始终不变色。
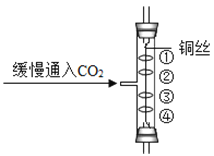
(4)能说明CO2密度比空气大的现象是____________________。
(5)①也能变红。说明微粒具有的性质是___________________。