题目内容
【题目】化学是以实验为基础的学科,结合图示两个实验回答有关问题:
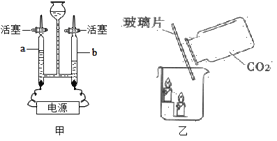
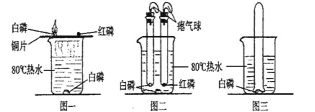
(1)用如图甲装置进行电解水的实验,b中收集到的气体是____________ ,该实验说明水是由 __________________组成的;
(2)在做如图乙实验时,观察到的现象为_____________________________________,说明CO2具有的性质是_____________________________________。
【答案】 氢气 氢元素和氧元素 低阶梯蜡烛先熄灭,高阶梯蜡烛后熄灭 既不能燃烧,也不能支持燃烧,且密度比空气的大
【解析】根据所学知识和题中信息知,(1)用如图甲装置进行电解水的实验,b中收集到的气体是氢气 ,该实验说明水是由氢元素和氧元素组成的;(2)在做如图乙实验时,观察到的现象为低阶梯蜡烛先熄灭,高阶梯蜡烛后熄灭,说明CO2具有的性质是既不能燃烧,也不能支持燃烧,且密度比空气的大。
点睛∶本题主要考查二氧化碳的性质。

【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)![]() 钠的氧化物
钠的氧化物![]() 氢氧化钠溶液
氢氧化钠溶液![]() 白色固体
白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:_______。
【实验探究一】:
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | __________ | 猜想1正确 |
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
实验操作 | 实验现象 | 实验结论 |
1.取少量白色固体加入足量____ | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入______ | 变成红色 |
【实验反思】
(1)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为_____.
(2)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2____碱性氧化物(填“是”或“不是”).