题目内容
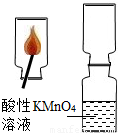
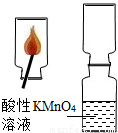
小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出。迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现紫红色KMnO4溶液褪色。

【提出问题】
问题1:火柴头的成分是什么?
问题2:什么气体使酸性KMnO4溶液褪色?
【查找资料】
小军从文献中查到:火柴头的主要成分为KClO3、硫黄粉(S)、三硫化二锑(Sb2S3)、玻璃粉等。
(1)写出火柴头燃烧时可能发生反应的化学方程式(要求写出两个):
①________________;②________________。
【实验探究1】
CO2气体是否能使酸性KMnO4溶液褪色?
(2)指明集气瓶中CO2的来源(答一种来源即可)___________________________________。
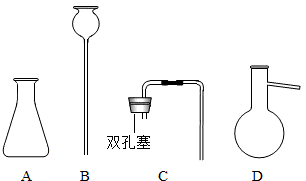
实验室提供了①稀硫酸、②块状碳酸钙、③稀盐酸、④碳酸钠固体等试剂及下列仪器。

(3 )请你从上述试剂和仪器中选择:最适合制备CO2气
)请你从上述试剂和仪器中选择:最适合制备CO2气 体的试剂(填序号)______;最适合制备CO2气体的仪器(填序号)______。
体的试剂(填序号)______;最适合制备CO2气体的仪器(填序号)______。
(4)请你指出仪器A的名称:______。
将制得的CO2气体通入酸性高锰酸钾溶液中,发现酸性高锰酸钾溶液不褪色。
【实验探究2】
SO2气体是否能使酸性高锰酸钾溶液褪色?
在老师的指导下,小军通过实验,验证了SO2气体可以使酸性KMnO4溶液褪色。
【讨论交流】
小军与其他同学通过讨论,提出了如下问题,请你帮助解决。
(5)SO2气体是大气污染物之一。SO2溶于雨水,通过进一步反应会形成酸雨。在我国,导致形成酸雨的SO2主要来自于(答一种来源即可)___________________________________。
(6)上述验证CO2不能使酸性KMnO4溶液褪色的实验过于复杂,请你设计一个更为简单的实验完成该实验:______________________。
解析:(1)KClO3受热产生KCl和O2,S和O2反应生成SO2。(2)火柴中有C、H等元素,燃烧产生CO2、H2O等。(3)实验室用石灰石(或大理石主要成分是CaCO3)和稀盐酸反应制CO2气体,不用Na2CO3的理由是反应速率太快,不利于收集;不用稀硫酸的理由是稀硫酸和块状CaCO3不能持续反应。(6)人呼出的气体中含有二氧化碳气体。
答案:(1)①2KClO3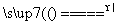 2KCl+3O2↑ ②S+O2
2KCl+3O2↑ ②S+O2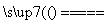 SO2
SO2
(2)火柴杆中含有碳元素,燃烧产生CO2
(3)②③ ABC
(4)锥形瓶
(5)煤的燃烧
(6)用导管向KMnO4溶液中吹气

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案 小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
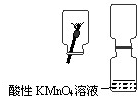 28、小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
28、小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.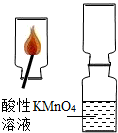 小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.
小军进行了下列实验:将数根火柴捆在一起,伸入到一集气瓶中,用另一根火柴点燃,等火柴头燃烧完后取出.迅速将集气瓶口与另一装有酸性KMnO4溶液的集气瓶瓶口对接,振荡,发现红色KMnO4溶液颜色消失.