题目内容
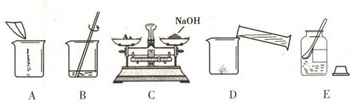
用固体氢氧化钠配制50g20%的氢氧化钠溶液时,应有①溶解②称量③计算④量取等操作步骤.其操作顺序正确的是
- A.③②④①
- B.③②①④
- C.①②③④
- D.②③④①
A
分析:配制一定溶质质量分数的氢氧化钠溶液,需要先计算出所需溶质与溶剂的量,而后进行根据所知的量进行称量、量取及溶解
解答:配制50g20%的氢氧化钠溶液时,需要先知道用溶质氢氧化钠多少克,溶剂水多少克,故首先是计算.计算完后,先称固体氢氧化钠,后量取水,最后是溶解,故步骤为:计算,称量,量取,溶解.
故选A.
点评:此题是对溶液配置实验的考查,重点复习配制溶液的步骤,对强化学生对溶液配制的知识有一定帮助
分析:配制一定溶质质量分数的氢氧化钠溶液,需要先计算出所需溶质与溶剂的量,而后进行根据所知的量进行称量、量取及溶解
解答:配制50g20%的氢氧化钠溶液时,需要先知道用溶质氢氧化钠多少克,溶剂水多少克,故首先是计算.计算完后,先称固体氢氧化钠,后量取水,最后是溶解,故步骤为:计算,称量,量取,溶解.
故选A.
点评:此题是对溶液配置实验的考查,重点复习配制溶液的步骤,对强化学生对溶液配制的知识有一定帮助

练习册系列答案
相关题目