题目内容
【题目】我国科研人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图所示,下列说法不正确的是( )
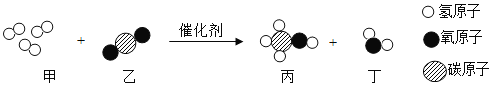
A.甲是单质,乙、丙、丁均为氧化物
B.反应前后氢元素的化合价发生了改变
C.参加反应的甲和乙的分子个数比为3:1
D.生成物丙和丁的质量比为8:9
【答案】AD
【解析】
由微观反应示意图可知,该反应的化学方程式为3H2+ CO2 CH3OH+H2O。
CH3OH+H2O。
A.丙物质的分子是由三种原子构成的,宏观上该物质是由三种元素组成的化合物,不属于氧化物,故A说法不正确;
B.该反应有单质氢气参加反应,反应前后氢元素的化合价发生了改变,故B说法正确;
C.由化学方程式可知,参加反应的甲和乙的分子个数比为3:1,故C说法正确;
D.由方程式可知,生成物丙和丁的质量比为32:18=16:9,故D说法不正确。
故选:AD。

 阅读快车系列答案
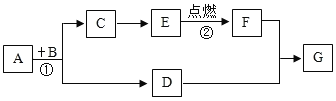
阅读快车系列答案【题目】某兴趣小组同学利用下图所示装置进行“铝与硫酸铜溶液反应”的实验时,发现反应后试管中的溶液出现分层现象:

【实验现象】
时间 | 观察现象 |
3min | 铝条表面有红色固体出现,铝条所在位置及其上方溶液颜色逐渐变浅,下方溶液没有变化 |
0.5h | 铝条表面聚集大量红色物质,铝条周围溶液呈无色透明,下方溶液仍为蓝色,无色溶液和蓝色溶液界面清晰 |
(1)写出铝和硫酸铜溶液反应的化学方程式___________________。
(2)实验前打磨铝条并将其绕成螺旋状的目的分别是_______________、_______________
(3)根据实验现象判断,铜与铝的金属活动性关系为___________________。
(4)根据反应后明显分层的溶液判断,生成的硫酸铝溶液密度_______(填“>”或“=”或“<”)原硫酸铜溶液密度,根据反应前后物质质量的关系分析,导致这种结果的原因可能是_______________。
附加分:若正确回答下列小题,将获得4分的奖励,但化学试卷总分不超过60分。
(5)为促进铝与硫酸铜溶液反应,在配制硫酸铜溶液时加入少量NaCl。
【提出问题】为什么在硫酸铜溶液中加入NaCl,有利于铝与硫酸铜溶液反应?
【提出假设】Cl的存在有利于铝与硫酸铜溶液反应。
【设计实验】请你设计一个合理的实验验证该假设_______________________________。
除以上方案外,你还能想到的另一种方案是_______________________________。
【题目】化学兴趣小组的同学欲用如图所示实验装置,通过实验探究质量守恒定律,根据实验目的,两位同学用了不同的药品进行实验,结果如下表所示:
所用药品 | 实验前后天平是否平衡 | |
小景 | 氯化钠溶液、硝酸钾溶液 | 平衡 |
小波 | 碳酸钙、稀盐酸 | 不平衡 |
(1)小景同学的天平一直平衡,他认为他的实验验证了质量守恒定律,但在小组讨论时,被同学指出设计错误,原因是_____。
(2)小波同学的实验中天平不平衡,你认为该反应是否_____(填“符合”、“不符合”之一)质量守恒定律,欲使反应前后天平平衡,可对该装置做的改进方法是_____
(3)化学反应前后,下列诸项中肯定没有变化的是_____(填A、B、C、D之一)
①原子的数目 ②分子的数目 ③元素的种类④原子的种类 ⑤物质的种类 ⑥分子的种类
A 只有①④⑥ B 只有①③④ C 只有①②④ D 只有②③⑥
(4)小玉同学做完了质量守恒定律的探究实验后,又欲测定一瓶标签破损的稀硫酸的溶质质量分数。她取了50g稀硫酸样品,逐滴加入10%的氢氧化钠溶液,用pH计测定溶液中pH变化如图所示,试回答:
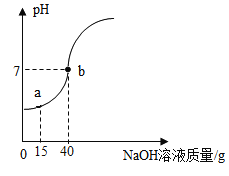
①当滴入氢氧化钠溶液15g时(即图中a点,烧杯内溶液中含有的溶质有_____、_____(写化学式)。
②计算所测稀硫酸的溶质质量分数_____(计算结果精确至0.1%)。
【题目】化学与人类生活息息相关。根据所学化学知识回答下列问题:
(1)如图是某校食堂周二午餐食谱的部分内容。
主食 | 米饭 |
副食 | 清蒸排骨、西红柿炒鸡蛋、咸味花生米 |
人体所需热量的60%~70%来自糖类,该食谱中富含糖类的食物是_____。
(2)走进厨房,你会发现煤气罐被管道天然气代替了,天然气属于_____能源(选填“可再生”或“不可再生”),其主要成分在空气中充分燃烧的化学方程式为_____。
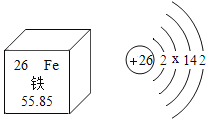
(3)使用铁强化酱油可预防贫血,铁属于人体所需的_____(选填“常量”或“微量”)元素;铁元素的原子结构示意图以及在元素周期表中信息如图,相对原子质量为_____,x=_____。
(4)加了洗涤剂的水洗涤油腻的碗筷既快捷又干净,这是由于洗涤剂具有_____功能。
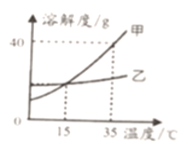
【题目】许多在水溶液的反应(如复分解反应),往往有易溶物转化为难溶物或难溶物转化为更难溶物的现象。下表为相同温度下某些物质的溶解度:
物质 | AgCl (白色) | Ag2S (黑色) | CaSO4 (白色) | Ca(OH)2 (白色) | Ca(HCO3)2(白色) | CaCO3 (白色) | (NH4)2SO4 无色透明 |
溶解度/g | 1.5×10-4 | 1.3×10-6 | 0.2 | 0.165 | 16.6 | 0.0015 | 75.4 |
(1)若在含有氯化银固体的水中加入硫化钠溶液,可能发生的现象是 _________。
(2)生产硫酸铵化肥的方法之一是:把石膏(CaSO42H2O)粉悬浮于水中,不断通入氨气再通入二氧化碳,充分反应后,立即过滤,滤液经蒸发而得到硫酸铵晶体。该反应的化学方程式为_____。
(3)从上表中再寻找两种能够按照上述规律相互转化的物质,写出实现该转化的化学方程式:______ 。