题目内容
实验室获取氮气有很多种途径,常见的3种方法是:
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气.
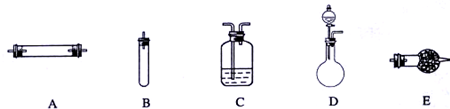
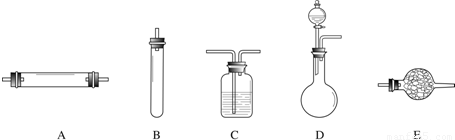
进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
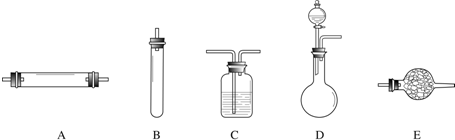
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置
(3)方法三:制氮气的化学方程式为:
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂.在制取氮气的3种方法中,联合使用方法一和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:
(5)1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右.若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气.
进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):

(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用
D
D
(选填装置编号).请写出生石灰在此反应中的两个作用:生石灰和水反应放热,促使氨水挥发、分解而得到氨气(或降低氨气的溶解度)
生石灰和水反应放热,促使氨水挥发、分解而得到氨气(或降低氨气的溶解度)
,生石灰与水反应,减少了溶剂
生石灰与水反应,减少了溶剂
.(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置
E
E
(选填装置编号)中加入碱石灰
碱石灰
以除去其它杂质气体.(3)方法三:制氮气的化学方程式为:
NaNO2+NH4Cl
NaCl+N2↑+2H2O
| ||
NaNO2+NH4Cl
NaCl+N2↑+2H2O
.
| ||
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂.在制取氮气的3种方法中,联合使用方法一和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
.(5)1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右.若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:
方法二制得的氮气中含有密度(或相对分子质量)比氮气大的稀有气体,导致密度偏大
方法二制得的氮气中含有密度(或相对分子质量)比氮气大的稀有气体,导致密度偏大
.分析:(1)根据反应物状态和反应条件选择发生装置,对比原料及生产过程分析生石灰的作用:生石灰和水反应生成熟石灰,一方面消耗氨水中的水,另一方面放出的热量促使氨水挥发、分解而得到氨气;(2)根据实验的要求要除去空气中多余的水蒸气、二氧化碳等杂质,可以通过碱性干燥剂完成;(3)根据反应物及题目的信息结合元素守恒判断生成物写出化学方程式;(4)根据绿色化学的定义结合反应的原理对比分析优点;(5)根据方法二得到的氮气不纯进行考虑.
解答:解:(1)用CaO和浓氨水反应,应选固液常温型的发生装置,即D;浓氨水常温下跟生石灰反应生成氨气和氢氧化钙,化学方程式为CaO+NH3?H2O=NH3↑+Ca(OH)2,因为氨水不稳定易挥发,生石灰和水反应生成熟石灰的过程中,生石灰的两个作用是:一方面消耗氨水溶液中的水,另一方面放出的热量促使氨水挥发、分解而得到氨气;
(2)空气中除了氮气、氧气外,还含有二氧化碳、水蒸气等,为保证所得氨气尽可能纯净,要除去空气中多余的水蒸气、二氧化碳等杂质,可以通过碱性干燥剂-碱石灰,既可以吸收二氧化碳又能吸收水;
(3)根据信息反应物是亚硝酸钠(NaNO2)和氯化铵,反应条件是加热,氮元素全部转化为氮气,反应前后元素的种类不变,因此生成物还有氯化钠和水,因此反应的方程式为:
NaNO2+NH4Cl
NaCl+N2↑+2H2O;
(4)从题中信息可知,NH3和CuO生成Cu和N2 而空气和Cu生成CuO,故Cu和CuO可以循环使用,方法三使用有毒的亚硝酸钠,方法一和二避免使用有毒物质而造成污染,因此联合使用方法一和方法二与单独使用方法三相比的优点有:铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染).
(5)将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末只是除去了氧气,其中还含有稀有气体等杂质,由于稀有气体的密度比氮气密度大,所以导致氮气密度总是偏大5‰左右.
故答案为:(1)D; 生石灰和水反应放热,促使氨水挥发、分解而得到氨气(或降低氨气的溶解度);生石灰与水反应,减少了溶剂;
(2)E;碱石灰; (3)NaNO2+NH4Cl
NaCl+N2↑+2H2O;(4)铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染);(5)方法二制得的氮气中含有密度(或相对分子质量)比氮气大的稀有气体,导致密度偏大.
(2)空气中除了氮气、氧气外,还含有二氧化碳、水蒸气等,为保证所得氨气尽可能纯净,要除去空气中多余的水蒸气、二氧化碳等杂质,可以通过碱性干燥剂-碱石灰,既可以吸收二氧化碳又能吸收水;
(3)根据信息反应物是亚硝酸钠(NaNO2)和氯化铵,反应条件是加热,氮元素全部转化为氮气,反应前后元素的种类不变,因此生成物还有氯化钠和水,因此反应的方程式为:
NaNO2+NH4Cl
| ||
(4)从题中信息可知,NH3和CuO生成Cu和N2 而空气和Cu生成CuO,故Cu和CuO可以循环使用,方法三使用有毒的亚硝酸钠,方法一和二避免使用有毒物质而造成污染,因此联合使用方法一和方法二与单独使用方法三相比的优点有:铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染).
(5)将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末只是除去了氧气,其中还含有稀有气体等杂质,由于稀有气体的密度比氮气密度大,所以导致氮气密度总是偏大5‰左右.
故答案为:(1)D; 生石灰和水反应放热,促使氨水挥发、分解而得到氨气(或降低氨气的溶解度);生石灰与水反应,减少了溶剂;
(2)E;碱石灰; (3)NaNO2+NH4Cl
| ||
点评:本题是一信息题,考查学生的知识拓展迁移能力,要求学生有良好的分析能力,能会从题干信息中找突破口,根据信息将学过的知识进行迁移

练习册系列答案
相关题目