题目内容
下表是元素周期表的一部分,请你据表回答问题.
(1)原子序数为16的元素是
(2)写出氧元素的原子结构示意图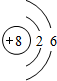
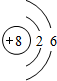
(3)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③
| 3Li 锂 6.941 |
4Be 铍 9.012 |
5B 硼 10.81 |
6C 碳 12.01 |
7N 氮 14.01 |
8O 氧 16.00 |
9F 氟 19.00 |
10Ne 氖 20.18 |
| 11Na 钠 22.99 |
12Mg 镁 24.31 |
13AI 铝 26.98 |
14Si 硅 28.09 |
15P 磷 30.97 |
16S 硫 32.06 |
17CI 氯 35.45 |
18Ar 氩 39.95 |
硫元素
硫元素
;该元素的化学性质与图中原子序数为8
8
的元素化学性质相似.该元素的原子在化学反应中易得到
得到
电子(填“得到”或“失去”).(2)写出氧元素的原子结构示意图
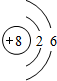
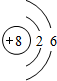
(3)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③
从左到右最外层电子数依次增加1
从左到右最外层电子数依次增加1
(任写一条).分析:(1)根据元素的化学性质决定因素和最外层电子数与得失电子的关系考虑;(2)根据原子结构示意图的画法考虑;(3)学会根据图表数据总结规律的方法.
解答:解:(1)左上角数字是该元素的原子序数,所以原子序数为16的元素是硫元素;决定元素化学性质的是原子的最外层电子数,硫最外层电子数是6,氧的最外层电子数也是6,所以硫元素和氧元素化学性质相似;
最外层电子数多于4个,易得电子,硫元素最外层电子数是6,所以易得到电子;
(2)第1层排满了只能排2个电子,第二层排满了最多排8个电子,因为氧的质子数是8,所以氧元素的原子结构示意图是: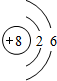
(3)同一横行属于1个周期,从左到右最外层电子数依次增加1;同一周期核外电子层数相同.
故答案为:(1)硫元素;8;得到;(2)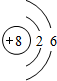 ;(3)从左到右最外层电子数依次增加1.
;(3)从左到右最外层电子数依次增加1.
最外层电子数多于4个,易得电子,硫元素最外层电子数是6,所以易得到电子;
(2)第1层排满了只能排2个电子,第二层排满了最多排8个电子,因为氧的质子数是8,所以氧元素的原子结构示意图是:
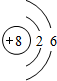
(3)同一横行属于1个周期,从左到右最外层电子数依次增加1;同一周期核外电子层数相同.
故答案为:(1)硫元素;8;得到;(2)
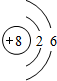 ;(3)从左到右最外层电子数依次增加1.
;(3)从左到右最外层电子数依次增加1.点评:解答本题关键是要知道决定元素化学性质的是原子的最外层电子数,熟悉最外层电子数多于4个易得电子,少于4个易失去电子.

练习册系列答案
相关题目
下表是元素周期表的一部分:
(1)16号元素的元素符号为 ;该元素的原子结构示意图如右,则X的数值= .
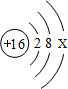
(2)8号元素和13号元素组成的化合物的化学式为 .
(3)请用表中的元素符号所组成的反应物写出符合要求的化学方程式:有水生成的化合反应: .
| 族 周期 |
IA | 0 | ||||||
| 一 | 1H 1,008 |
ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2He 4,003 |
| 二 | 3Li 6,941 |
4Be 9,012 |
5B 10,81 |
6C 12,01 |
7N 14,01 |
8O 16,00 |
9F 19,00 |
10Ne 20,18 |
| 三 | 11Na 22,99 |
12Mg 24,31 |
13Al 26,98 |
14Si 28,09 |
15P 30,97 |
16S 32,06 |
17Cl 35,45 |
18Ar 39,95 |
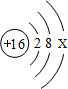
(2)8号元素和13号元素组成的化合物的化学式为
(3)请用表中的元素符号所组成的反应物写出符合要求的化学方程式:有水生成的化合反应:


 ,则m=
,则m=
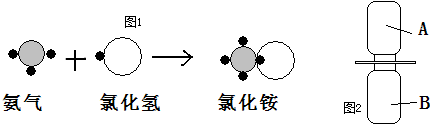
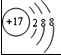 表示的是
表示的是 ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图1表示:
”表示氯原子,上述反应过程可用图1表示: