题目内容
【题目】在木炭还原氧化铜的实验中:
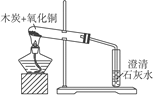
(1)反应开始后,在盛澄清石灰水的试管中观察到的现象是________________,说明反应中有_______生成,被加热的试管中发生的化学反应方程式是______________。
(2)反应完成后,把被加热的试管里的粉末倒在纸上可以看到有____色的铜,这是由于_。
(3)右图中酒精灯上加一金属网罩的作用__________________________。
(4)实验结束时,应先_____________,再撤掉____________
【答案】(1)澄清石灰水变浑浊二氧化碳
C+2CuO![]() 2Cu+CO2↑
2Cu+CO2↑
(2)亮红 木炭有还原性,能与氧化铜反应,生成金属铜
(3)使酒精灯的火焰集中,使被加热部位的温度更高
(4)把导气管从澄清石灰水中移出酒精灯
【解析】
(1)反应开始后,观察到澄清的石灰水变浑浊,说明木炭与了氧化铜反应生成了二氧化碳,方程式是:C+2CuO![]() 2Cu+CO2↑;(2)反应完成后,把被加热的试管里的粉末倒出,可以看到有红色的铜,是由于木炭还原氧化铜生成了红色的铜,说明木炭具有还原性;(3)酒精灯火焰加上网罩后火焰会集中,从而提高了火焰的温度;(4)实验结束要先移导管后熄灯,防止石灰水倒吸引起试管炸裂。
2Cu+CO2↑;(2)反应完成后,把被加热的试管里的粉末倒出,可以看到有红色的铜,是由于木炭还原氧化铜生成了红色的铜,说明木炭具有还原性;(3)酒精灯火焰加上网罩后火焰会集中,从而提高了火焰的温度;(4)实验结束要先移导管后熄灯,防止石灰水倒吸引起试管炸裂。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
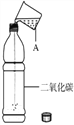
【题目】小乐利用图示实验装置测定某大理石样品的纯度(所含杂质不与盐酸反应,且不溶于水)。她取了该大理石样品12.5g,并加入足量稀盐酸进行实验。实验数据记录如下表:
时间/s | 0 | 20 | 30 | 40 |
装置和药品的总质量/g | 117.9 | 114 | 113.5 | 113.5 |

(1)反应共生成CO2的质量为______g。
(2)计算该大理石样品中CaCO3的质量分数______。(写出计算过程)