题目内容
【题目】大规模利用电解水制取氢气,技术瓶颈是如何降低电能消耗,从而大幅降低制氢成本。如图甲是电解水的简易装置,图乙为电解水生成的气体体积与时间关系图,请回答完成下列问题:
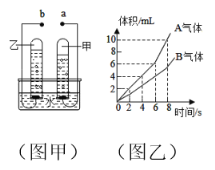
(1)在该实验中,通常会加入少量的硫酸钠或氢氧化钠的目的是________________。若甲管生成气体A,则b应接电源___极。
(2)若乙管生成气体B用带火星检验,产生的现象为_______,说明气体具有的性质为____。
(3)当4分钟后,甲、乙试管排出水的体积比为___。该反应的化学方程式表达式(为_________,该反应的基本类型为____________。
(4)该实验得出的一个结论为__________________________。
【答案】增强水的导电性 正 带火星的木条复燃 助燃性 2:1 2H2O![]() 2H2↑+O2↑ 分解反应 水是由氢、氧元素组成的;化学反应中,分子可分而原子不可分(或化学变化的实质是反应物分子破裂成原子,而原子重新组合新的分子)等
2H2↑+O2↑ 分解反应 水是由氢、氧元素组成的;化学反应中,分子可分而原子不可分(或化学变化的实质是反应物分子破裂成原子,而原子重新组合新的分子)等
【解析】
电解水负极生成氢气,正极生成氧气,氢气和氧气的体积比是2:1。
(1)在该实验中,通常会加入少量的硫酸钠或氢氧化钠,硫酸钠电离出钠离子和硫酸根离子,氢氧化钠电离出钠离子和氢氧根离子,故目的是增强水的导电性。若甲管生成气体A,生成的气体较多,为氢气,连接负极,则b应接电源正极。
(2)若乙管生成气体B是氧气,具有助燃性,用带火星检验,产生的现象为带火星的木条复燃,说明气体具有的性质为助燃性。
(3)电解水负极生成氢气,正极生成氧气,氢气和氧气的体积比是2:1,当4分钟后,甲试管生成氢气,乙试管生成氧气,故甲、乙试管排出水的体积比为2:1。该反应的化学方程式为2H2O![]() 2H2↑+O2↑,反应符合一变多的特点,故该反应的基本类型为分解反应。
2H2↑+O2↑,反应符合一变多的特点,故该反应的基本类型为分解反应。
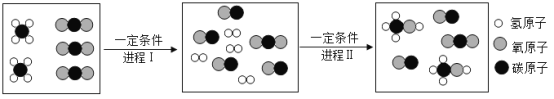
(4)该实验得出的结论为水是由氢、氧元素组成的;化学反应中,分子可分而原子不可分(或化学变化的实质是反应物分子破裂成原子,而原子重新组合新的分子)等。

 名校课堂系列答案
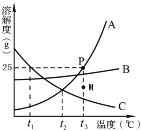
名校课堂系列答案【题目】KNO3和KCl在不同温度时的溶解度如表所示.请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度 | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
(1)由表中数据分析可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是______.
(2)10℃时,131g饱和KCl溶液,蒸发10g水后,再降温到10℃,可析出KCl晶体的质量为______.
(3)如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的______(填字母序号).
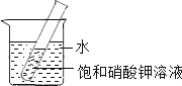
a.氢氧化钠固体 b.生石灰固体 c.硝酸铵固体