题目内容
【题目】已知相同条件下,气体的体积比等于气体的分子个数比。现有20 mLO2、CO和CO2的混合气体,在密闭容器中用电火花引燃,充分反应后恢复到原来状态,体积减少了2 mL,再通过足量澄清石灰水后又减少10mL,最后剩余气体能使带火星的木条复燃。原混合气体中O2、CO和CO2的体积比可能是
A.1:6:3
B.5:2:3
C.3:1:6
D.3:5:2
【答案】B
【解析】
已知相同条件下,气体的体积比等于气体的分子个数比。在密闭容器中用电火花引燃,充分反应后恢复到原来状态,体积减少了2 mL。则有:
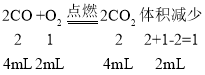
由上述关系可知,生成的二氧化碳的体积为4mL,原来混合气体中二氧化碳的体积=10mL-4mL=6mL,一氧化碳和氧气的体积为:20mL-6mL=14mL。由题意可知,最后剩余气体能使带火星的木条复燃,说明了一氧化碳完全反应,剩余的气体是氧气。 则氧气体积为:14mL-4mL=10mL,则原来混合气体中O2、CO、CO2的体积比是:10mL:4mL:6mL=5:2:3;故选B。

练习册系列答案
相关题目