题目内容
【题目】兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题。
(1)配制30g 10%的Na2CO3溶液。量取蒸馏水所需量筒的规格是 (从10、50、100中选择)mL。最后将碳酸钠溶液转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是 (填序号)。
A.30g B.10% C.Na2CO3溶液
(2)测定未知浓度Ba(OH)2溶液的溶质质量分数。取50g Ba(OH)2溶液,逐滴滴加上述Na2CO3溶液的过程中,测得产生沉淀与加入Na2CO3溶液的质量关系如图所示。
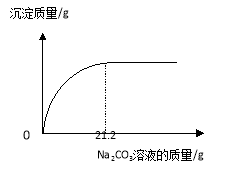
①恰好完全反应时,消耗Na2CO3溶液的质量为 g。
②请通过计算确定Ba(OH)2溶液的溶质质量分数。
已知:Ba(OH)2+ Na2CO3=BaCO3↓+2NaOH。
【答案】(1)50 A(2)① 21.2 ② 6.84%
【解析】
试题分析:(1)根据溶质质量分数计算表达式的变形,配制30g10%的Na2CO3溶液需要碳酸钠的质量=30g×10%=3g,水的质量=30g-3g=27g,量取蒸馏水所需量筒的规格是50 ;标签上应书写的内容:溶液的名称以及溶质质量分数,溶液的质量在标签上可以不必注明,故选A
(2)①根据图像,恰好完全反应时,消耗Na2CO3溶液的质量为21.2g
② 根据化学方程式:Ba(OH)2+Na2CO3==BaCO3↓+2NaOH中Na2CO3与Ba(OH)2的质量关系,可求出Ba(OH)2的质量,进一步计算Ba(OH)2溶液的溶质质量分数
解:设Ba(OH)2的质量为x
Ba(OH)2+Na2CO3==BaCO3↓+2NaOH
171 106
x 21.2g×10%
171:106=x: 21.2g×10%
x=3.42g
Ba(OH)2溶液的溶质质量分数=3.42g/50g×100%=6.84

 出彩同步大试卷系列答案
出彩同步大试卷系列答案





